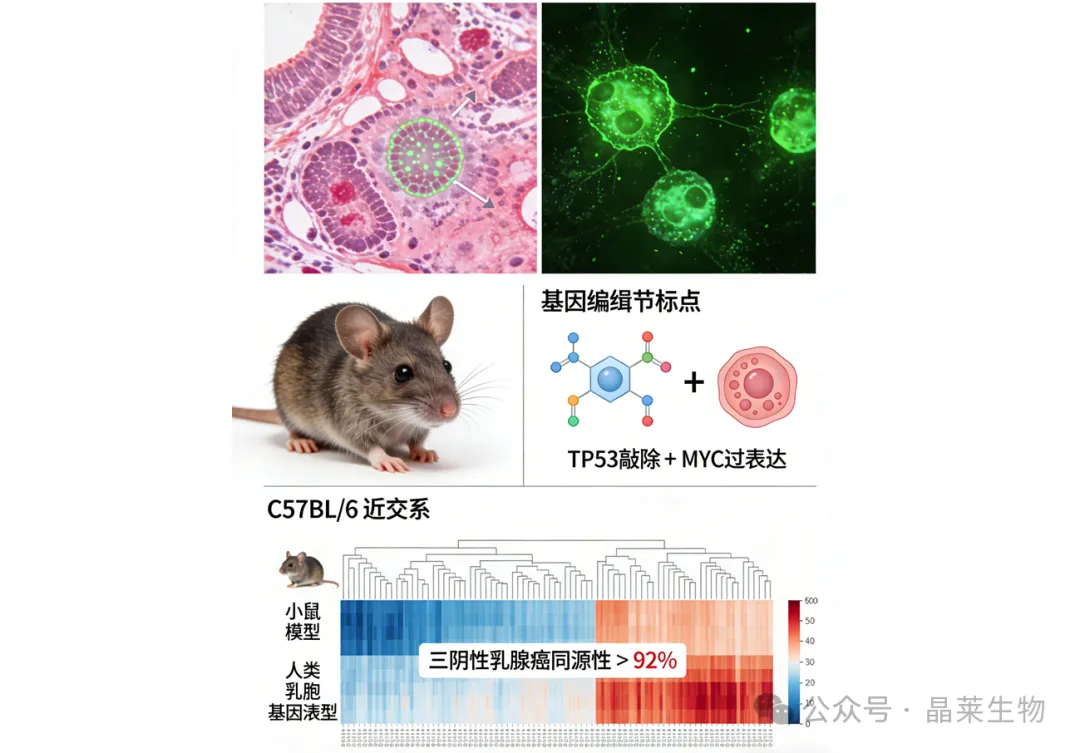
全球每29秒就有1例乳腺癌新发病例。 曲妥珠单抗、帕博利珠单抗等抗癌 “明星药”,无一不是先在小鼠身上证实疗效,才踏上拯救人类的征程。 同样是乳腺癌,为何跨物种的研究能实现 “鼠身试药,人类受益”? 这背后既藏着生命进化的密码,更离不开科研人员对实验模型的精准构建与科学转化 —— 今天,我们就从分子机制到临床应用,拆解这跨越物种的 “抗癌桥梁”。 生命密码的高度契合: 小鼠与人类乳腺癌的 “同源性基础” 乳腺癌并非单一疾病,而是由数十种分子亚型构成的复杂疾病谱 —— 从激素受体阳性型到 HER2 富集型,再到预后最差的三阴性乳腺癌,不同亚型的致病基因、信号通路和治疗响应差异巨大。 实验小鼠之所以能成为靠谱 “替身”,核心在于物种间的基因保守性:小鼠与人类共享 85% 以上的编码基因,而乳腺癌相关关键基因(如 TP53、MYC、HER2)的功能一致性更是高达 90% 以上。 2026 年《Transcriptomic classification》的重磅研究进一步证实: 通过基因工程构建的 27 种小鼠乳腺癌模型中,8 种能精准模拟人类特定亚型的转录组特征: TRP53 基因敲除小鼠的肿瘤剖面 → 与人类基底样乳腺癌(三阴性乳腺癌的主要亚型)的分子图谱几乎重合; WAP-Cre-ETV6 转基因小鼠 → 完美复现了 HER2 富集型乳腺癌的恶变进程。 这种 “亚型精准匹配”,让小鼠身上的肿瘤生长、侵袭转移、药物反应,都能最大程度贴近人类临床场景,为后续转化研究筑牢了核心基础。 可控的 “疾病全景实验室”: 小鼠模型的三大不可替代优势 与临床患者存在的个体差异(年龄、基础疾病、基因背景混杂)相比,实验小鼠为乳腺癌研究提供了 “理想化研究场景”,其优势堪称 “天然实验室”: 1.遗传背景均一性: 近交系小鼠(如 C57BL/6、BALB/c)经过多代培育,基因相似度达 99.9% 以上,能彻底排除个体差异干扰 —— 同一批小鼠接受同一药物治疗,结果可重复性远超临床患者队列,让药物疗效、基因功能的评估更精准; 2.疾病进程可追溯: 借助 CRISPR-Cas9、转基因等技术,可在小鼠体内 “定向诱导” 乳腺癌发生:从正常乳腺细胞恶变,到肿瘤侵袭周围组织,再到远处转移(如肺、骨转移),全过程可通过活体成像实时监测,这在人类临床中完全无法实现; 3.伦理与效率平衡: 小鼠繁殖周期仅 3-4 个月,单窝可产 6-10 只幼鼠,能在短期内完成大样本量的药物筛选、剂量优化和毒性测试 —— 一款抗癌药在小鼠模型中完成初步验证仅需 6-12 个月,而临床前人体相关研究往往需要数年,这种效率是临床研究难以企及的。 从小鼠到病床: 乳腺癌治疗的每一次进步,都离不开动物实验 回顾近三十年乳腺癌诊疗的里程碑突破,几乎每一项都建立在小鼠模型的研究之上: 每一项在小鼠身上完成的机制验证、药物筛选、剂量探索、毒理评估,都为临床研究扫清了最危险、最未知的障碍。我们今天在临床上使用的每一种标准方案,都曾在小鼠体内被反复验证。 小鼠身上的数据,最终变成患者的生存期与生活质量。 科学严谨性: 模型选择与动物福利的双重保障 值得强调的是,小鼠研究的转化价值,离不开严格的科学规范与伦理约束: 1. 模型精准匹配原则: 研究者需根据研究目的选择合适模型 —— 基础机制研究常用基因工程小鼠,药物临床前评价优先采用 PDX 模型(直接移植患者肿瘤组织,更贴近临床场景),避免 “模型错配” 导致的转化失败; 2.动物福利合规性: 所有实验均需通过机构伦理委员会审批,严格遵循“3R原则”(替代、减少、优化):小鼠饲养环境符合GB14925国家标准,实验操作采用麻醉镇痛,术后给予护理,最大程度减少动物痛苦; 3.多模型交叉验证: 重要研究结果必须在至少两种不同小鼠模型中验证,同时结合细胞实验、类器官模型数据,避免单一模型的局限性,确保研究结论的可靠性。 从实验室里的小鼠笼到医院的治疗床,这看似跨越物种的研究,实则是对生命机制的深刻解码。 小鼠以其独特的生物学优势,成为乳腺癌研究中不可替代的 “活试剂”——它不仅帮助我们破解疾病奥秘,更搭建了从基础研究到临床治愈的关键桥梁。 每一只实验小鼠的付出,都在为人类抗癌事业积累力量;每一项在小鼠身上取得的突破,都是向拯救更多乳腺癌患者迈出的坚实一步。 作为科研工作者,我们既要尊重实验动物的贡献,更要坚守科学严谨性,让更多 “鼠身研究” 转化为临床良药,这正是这份事业的温度与重量。 关于晶莱