

肿瘤药物研发是一场从实验室到临床的接力赛,而动物模型的选择,往往决定了这场接力能否顺利交接。
选错模型,可能让一个有潜力的候选药物在起点就被误判;选对模型,则能在正确的阶段回答正确的问题,大幅提升研发效率。
这篇文章,帮你理清不同阶段该用什么模型、用多少模型,以及为什么这样选。
肿瘤动物模型主要涵盖五大类型,每种模型都有其独特的应用场景和优劣势:
1.异位异种移植瘤模型
将肿瘤细胞系或组织外植体,通过皮下(sc)、腹腔(ip)、静脉(iv)、肌肉(im)等途径,移植到同基因或免疫缺陷的啮齿类宿主体内。
2.原位模型
将肿瘤组织外植体或已建立的肿瘤细胞系,植入肿瘤起源的对应器官或组织内,从而重现原发肿瘤生长、侵袭与播散所处的局部微环境,以及其中复杂的细胞间相互作用。
3.种系转基因与条件性转基因模型(GEMMs)
可对特定癌基因或抑癌基因的表达模式进行全身性调控,或实现组织、时间特异性的调控。
4.人源原发肿瘤移植瘤模型
可保留其来源原发肿瘤的基因型与表型特征。
5.多种致癌物诱导模型
可重现环境致癌物与促癌物作用下,肿瘤发生呈时间依赖性的多阶段进展过程。
临床前癌症模型共分为五类,各类模型在研发中的应用场景、核心优势、局限性存在显著差异,临床预测价值也随模型复杂度和生理学相关性逐级提升,是药物研发中不同阶段的关键工具,具体细节如下:

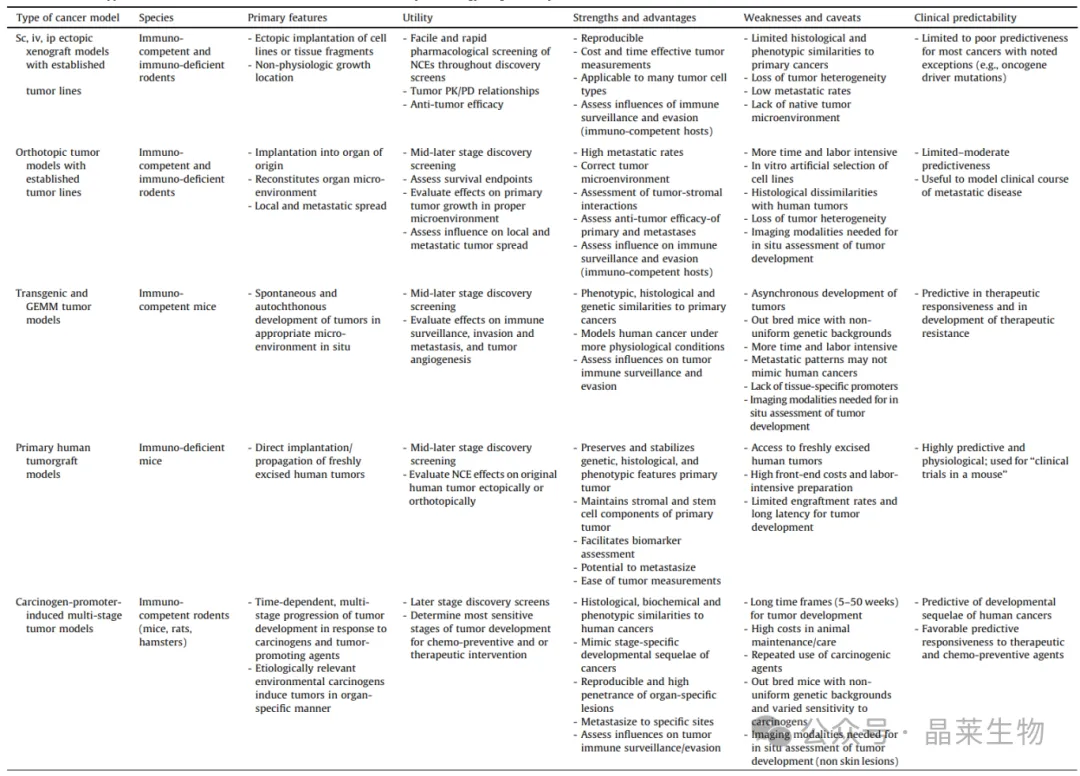
药物研发是从早期筛选到临床前验证的迭代式过程,模型的选择、使用数量与阶段直接取决于待解决的科学问题。
核心原则:从简单到复杂、从低生理相关性到高生理相关性。
根据研发阶段的核心目标选择单一或多种模型组合,避免孤立使用某一类模型。
核心目标
快速确定新化学实体的肿瘤PK/PD关系,评估其体外/体内抗肿瘤疗效与整体耐受性,完成初筛与汰选。
模型选择
首选异位肿瘤异种移植模型,可单独使用或构建多肿瘤细胞系的模型面板;若研究靶点与免疫相关,可同时在免疫缺陷/健全小鼠中构建模型,初步评估免疫对药物的影响。
使用数量
选择覆盖不同癌种、不同基因型的多种肿瘤细胞系构建模型,保证筛选的广谱性;每个新化学实体至少在3-5种相关模型中完成评估。
核心作用
快速淘汰无效化合物,筛选出具有潜在抗肿瘤活性的候选物,为后续研究奠定基础。
核心目标
优化先导化合物的药学性质,明确其剂量-效应关系、给药方案,研究药物对肿瘤侵袭、转移、血管生成的作用,初步评估药物的联合治疗潜力。
模型选择
以原位肿瘤模型为主,结合异位模型进行补充;若研究靶点与肿瘤-基质相互作用、免疫相关,优先选择免疫健全小鼠的同基因原位模型;若靶点为特定致癌驱动基因,可结合对应的GEMMs进行机制验证。
使用数量
选择1-2种与临床适应症最相关的原位模型,搭配2-3种异位模型进行剂量优化;联合治疗研究需在至少2种模型中验证,保证结果的可靠性。
核心作用
优化先导化合物的研发策略,明确其潜在的临床应用场景,为进入后期验证提供依据。
核心目标
全面评估候选药物的疗效、安全性、耐药机制,确定临床给药剂量/方案,探索联合治疗策略,鉴定肿瘤特异性生物标志物,为临床试验提供完整的转化药理学数据。
模型选择
以GEMMs和人源原发肿瘤移植瘤模型为核心,搭配致癌物诱导模型(若用于预防/早期干预)进行补充;原位模型可作为辅助,评估药物对转移瘤的疗效与生存获益。
使用数量
选择2-3种临床相关性高的GEMMs(覆盖不同基因型/癌种)和5-10种人源原发肿瘤移植瘤模型(匹配临床患者人群);联合治疗研究需在多种模型中验证,确保方案的合理性。
核心作用
完成候选药物的临床前全面验证,为临床试验的设计(如患者入组标准、给药方案、生物标志物检测)提供直接依据,降低临床研发失败风险。
核心目标
验证候选药物的临床转化价值,优化临床试验方案,开展"共临床试验",实现临床前研究与临床研究的实时迭代。
模型选择
首选人源原发肿瘤移植瘤模型和特定癌种的GEMMs,这两类模型是"小鼠体内临床试验"的核心工具;若药物用于肿瘤预防,可搭配致癌物诱导的多阶段模型。
使用数量
选择与临床试验入组人群高度匹配的人源原发肿瘤移植瘤模型面板(不少于10种),结合1-2种代表性GEMMs;实现临床方案与小鼠模型研究方案的同步,保证数据的可比性。
核心作用
提前预测候选药物的临床疗效与耐药人群,优化临床试验的入组标准和给药方案,提升临床试验的成功率,弥合临床前研究与临床研究的转化鸿沟。
1. 免疫相关靶点?尽早引入原位模型和GEMMs
若研究分子靶点/通路与肿瘤侵袭、转移、血管生成、免疫相关,需在研发中期尽早引入原位模型、GEMMs(免疫健全宿主),避免仅使用异位模型导致的结果偏差。
2. 上临床前必须过的一关
所有候选药物在进入临床试验前,必须在人源原发肿瘤移植瘤模型中完成验证,确保其临床相关性。
3. 不要依赖单一模型
单一模型无法全面反映人类癌症的异质性,后期研发阶段需采用多种模型组合,综合评估药物的疗效与安全性,避免孤立解读某一类模型的结果。
4. 样本量要够
模型的使用数量需根据研究的统计效力确定,核心研究(如疗效、耐药机制)需保证足够的模型数量,确保结果的可靠性。
5. 让模型服务于科学问题
模型选择的核心逻辑始终是:先想清楚要解决什么科学问题,再选择能回答这个问题的模型,而不是反过来。
结语
肿瘤动物模型的选择,本质上是在"效率"与"相关性"之间寻找平衡。
早期要快,后期要准。没有最好的模型,只有最适合当前阶段的模型组合。
希望这份指南,能为你的研发决策提供一份清晰的参考地图。
关于晶莱
