

谁懂啊家人们!做WB实验最崩溃的瞬间,除了跑胶漏液、转膜掉胶,还有辛辛苦苦熬到显影,结果条带糊成“马赛克”,要么背景高到发亮,目标条带直接被“淹没”——反复返工、换试剂,却还是踩坑不断,时间和样品全白费!
其实WB条带弥散、背景太高,根本不是你“手气差”,而是实验全流程里藏着很多容易被忽略的小细节,今天就拆解8个新手必踩的坑,搭配对应解决方案,帮你快速避坑、一次跑出清晰条带,少走弯路。
条带弥散、拖尾、不成形,甚至Marker都跑歪,大概率是这几个环节没做好,对照自查,秒找问题根源。
很多人图省事,样品裂解后不离心、煮样时间不够,或者Loading buffer加少了——结果蛋白变性不彻底、杂质过多,跑胶时无法整齐迁移,条带直接“散开”,甚至出现哑铃状、梯形条带。
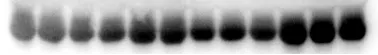
正确操作:样品冰上裂解,低温超声后,加入足量Loading buffer,100℃煮10-15min,12000rpm离心5-10min,只取上清上样,杜绝杂质干扰。
坑2:电泳缓冲液“反复利用”
为了节省试剂,电泳缓冲液反复用3次以上,甚至不更换——久而久之,缓冲液中SDS失效、离子浓度失衡,电泳时电场不均匀,蛋白迁移速度不一,条带自然弥散、弯曲,还可能出现纵向纹理。
正确操作:内槽每次用新鲜电泳液,外槽缓冲液最多回收2-3次;若条带整体弯曲,可适当降低电泳电压,电泳时冰浴降温,减少边缘效应。
转膜时三明治结构没装紧,胶和膜之间有气泡,或者转膜液没浸没胶膜、产热过多——导致蛋白转印不均匀,Marker条带不成形,目标条带弥散模糊,甚至出现重影。
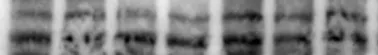
正确操作:PVDF膜先用预冷甲醇激活,装三明治结构时,用滚轮擀去所有气泡,确保胶、膜、滤纸紧密贴合;转膜全程冰浴,保证转膜液充分浸没,避免产热影响条带形态。
坑4:上样量“贪多”,泳道“超负荷”
总觉得“上样量越多,信号越强”,盲目加样过多——结果蛋白过载,泳道拥挤,蛋白无法正常分离,条带连成一条线,甚至拖尾严重,反而看不到清晰的目标条带。

正确操作:根据胶的孔径和样品浓度调整上样量,常规3.5mm胶孔建议上样20-30μg蛋白,体积不超过20μL;若样品蛋白浓度高,可适当稀释,或间隔上样减少粘连。
背景太高“亮如灯泡”?
这4个坑别再踩!
显影后膜上一片发亮,目标条带被杂带掩盖,甚至出现黑色小颗粒,核心是“非特异性结合”,问题全在这4个环节。
封闭液用量不足、时间太短,或者封闭液反复使用——膜上的空白位点没被完全阻断,一抗、二抗会非特异性结合,导致背景整体偏高,甚至出现不均匀斑点。
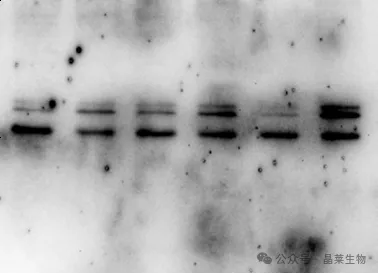
正确操作:常规蛋白用脱脂牛奶封闭,修饰型蛋白(如磷酸化蛋白)用BSA封闭;封闭液现配现用,用量以完全覆盖膜为宜,室温封闭2小时以上或4℃过夜,避免反复使用。
严格按照说明书稀释抗体就够了,但很多人担心信号弱,刻意提高抗体浓度,或延长孵育时间——导致抗体过量,非特异性结合增加,背景飙升,甚至条带泛白过曝。
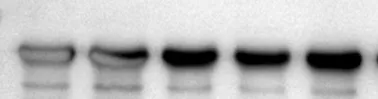
正确操作:一抗、二抗按说明书比例梯度优化,一抗4℃孵育过夜(减少非特异性结合),二抗室温孵育1小时即可,避免过量孵育。出现反白情况,尝试稀释发光液,或者将膜浸泡过夜。
孵育后洗膜次数太少、时间太短,摇床转速太低——游离的一抗、二抗残留在膜上,显影时会产生背景信号,甚至出现杂带,这是最容易被忽略的“小坑”!
正确操作:用含0.1%-0.2%Tween-20的TBST洗膜,每次10-15分钟,共4-5次,提高摇床转速(60-80rpm),确保膜的每个区域都被充分洗涤;最后一次可用TBS洗,避免Tween-20干扰显影。
发光液滴加过多,或曝光时间太长——哪怕条带信号足够,背景也会被过度放大,导致膜整体发亮,目标条带模糊;甚至Marker被过度曝光,干扰结果判读。

正确操作:发光液滴加量以刚好覆盖膜为宜,滴加后静置1分钟,吸去多余液体再显影;采用梯度曝光(10秒、30秒、1分钟),选择最佳曝光时长,避免过曝。
其实WB实验没有“玄学”,条带弥散和高背景的核心问题,总结起来就3点:
1.样品处理不规范——裂解、煮样、离心每一步都要到位
2.试剂使用不当——所有缓冲液现配现用,避免反复使用
3.操作细节疏忽——低温处理、均匀贴合、充分洗涤是关键
记住这几个关键原则:
• 所有缓冲液(电泳液、转膜液、封闭液)尽量现配现用
• 全程注重"低温"和"均匀":样品低温处理、转膜冰浴、一抗4℃孵育
• 胶膜贴合均匀、洗膜均匀、发光液滴加均匀
结语
最后想说,做WB难免踩坑,不用焦虑!
对照上面的坑自查,逐一优化操作,大多数条带问题都能解决,如果还是没头绪,评论区留言你的具体情况,一起交流避坑技巧~
关于晶莱
