

在细胞生物学研究中,细胞凋亡(Apoptosis)的检测是绕不开的经典实验。而在众多检测方法中,TUNEL染色因其能够原位直观地检测DNA断裂情况,被视为细胞凋亡检测的“金标准”之一。
虽然原理简单,但做过的小伙伴都知道:TUNEL容易做,但做好很难! 假阳性、高背景、不显色……各种问题层出不穷。
今天,小晶就结合一份详尽的实验笔记,为大家梳理TUNEL染色的全流程及关键注意事项。
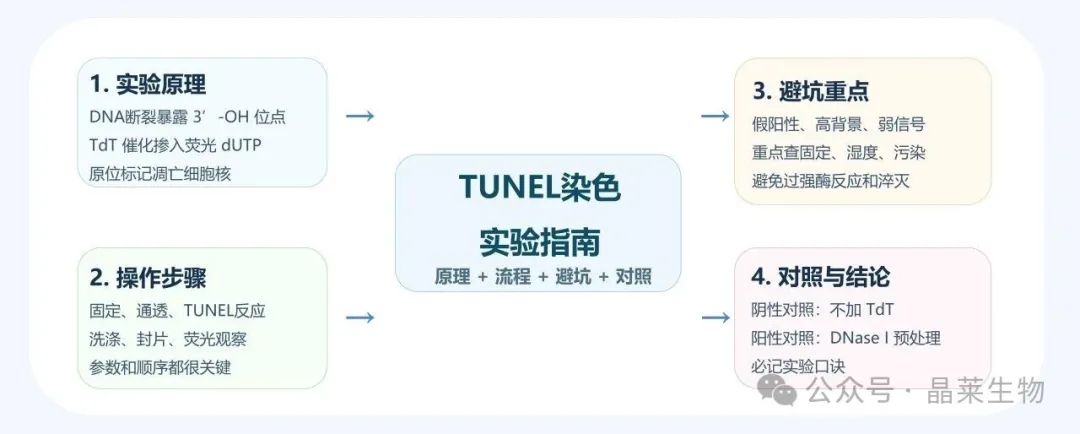
当细胞发生凋亡时,内源性核酸内切酶被激活,它们像剪刀一样将基因组DNA切断,形成180-200bp的DNA片段。
TUNEL技术可利用末端脱氧核苷酸转移酶(TdT),专门识别这些断裂DNA暴露出来的3’-OH末端,并将带有荧光标记的dUTP“粘贴”上去。

1. 细胞固定
操作:使用 4%多聚甲醛 (PFA) 固定细胞 30分钟。
目的:保持细胞形态,防止DNA片段丢失。
2. 通透处理
操作:PBS洗涤后,加入含 0.3% Triton X-100 的PBS,室温孵育 5分钟。
目的:像给细胞膜打孔,让检测试剂能进入细胞核与DNA结合。
3. TUNEL反应
配液:按照试剂盒说明配制TUNEL检测液。
孵育:样品上加50μl检测液,37ºC 避光孵育 60分钟。
用量参考:96/48/24/12孔板及切片一般用50μl;6孔板建议用100μl。
环境保湿:孵育盒或孔板空隙中务必加水,保持湿润环境。
4. 终止与观察
操作:PBS洗涤3次,洗去未结合的荧光探针。
封片:使用含抗荧光淬灭剂的封片液(通常含DAPI复染细胞核)封片,荧光显微镜观察。

问题一:出现大量非特异性荧光(假阳性)
1. 内源性酶干扰
某些高酶活性的组织(如平滑肌),自身的核酸酶会切割DNA。
解决方案:取材后立即固定,且固定要充分,锁死酶活性。
2. 固定液PH值不对
使用了酸性固定液。
解决方案:必须使用PH中性的缓冲福尔马林或4%多聚甲醛。
3. 样品干涸:反应过程中液体流失或蒸发,导致非特异性吸附。
解决方案:严格保湿!可参考“防蒸发小技巧”
防蒸发小技巧:
方法A:使用防蒸发膜。
方法B:裁剪比孔略小的圆形塑料片(或自封袋膜),滴加检测液后覆盖在样品上。这不仅能防止蒸发,还能让液体铺得更均匀。
Tip:裁剪时留个小“把手”,染色结束后方便镊子夹取。
方法C:载玻片可用PAP Pen画圈圈住液体。
问题二:荧光背景过高,甚至细胞质也发光
1. 支原体污染
支原体的DNA也会断裂被标记。
解决方案:实验前务必进行支原体检测。
2. TdT酶浓度过高
反应过强。
解决方案:尝试用稀释液将TdT酶稀释2-5倍后使用。
3. 红细胞干扰
血红蛋白有自发荧光。
解决方案:处理组织样本时,尽量去除红细胞。
问题三:标记效率低,甚至无荧光
1. 固定剂选错
使用了乙醇或甲醇。
解决方案:它们会漏掉小片段DNA,请换回4%多聚甲醛。
2. 固定时间过长
导致交联过度,试剂进不去。
解决方案: 缩短固定时间,或延长通透时间(用蛋白酶K消化时需谨慎控制)。
3. 荧光淬灭
FITC对光敏感,普光照10分钟就可能淬灭。
解决方案:全程避光!避光!避光!
4. 细胞被洗掉了(尤其是贴壁细胞)
凋亡的细胞贴壁能力变弱,一洗就掉。
解决方案:诱导凋亡结束后,先用平底转子离心机 1000g 离心 5分钟,把快飘起来的凋亡细胞“压”回去,再吸除培养基。后续洗涤动作一定要轻柔。
5. 特别注意
如果你使用碘化丙啶(PI)染细胞核,PI颜色过深会淬灭FITC的绿色荧光(能量转移)。
解决方案:降低PI浓度(如0.5μg/ml),或者改用DAPI(蓝色)复染细胞核,蓝绿搭配对比度更好。

为了确保实验结果的可信度,强烈建议在正式实验中设置对照组:
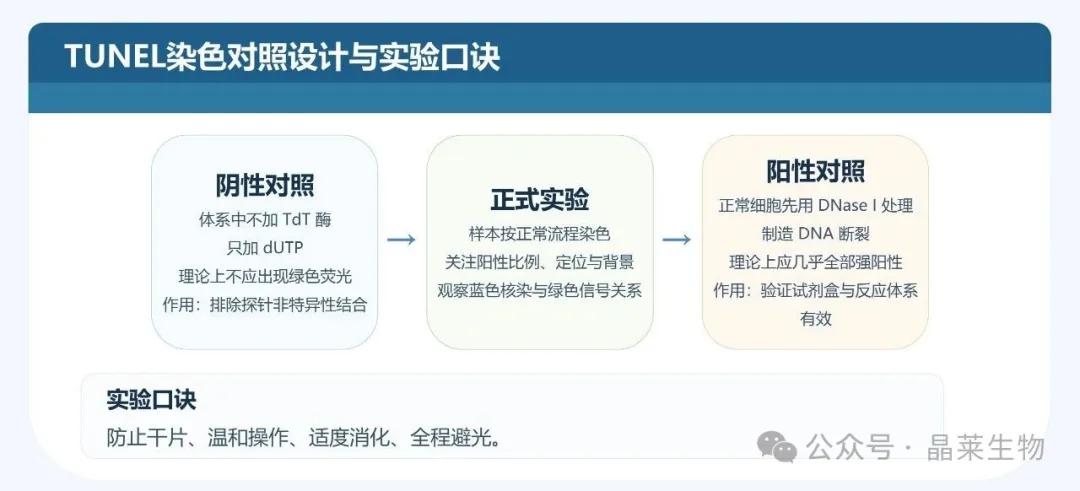
阴性对照:反应液中不加TdT酶,只加dUTP。理论上应无绿色荧光。
目的:排除试剂本身的非特异性结合。
阳性对照:使用DNase I处理正常细胞10-30分钟,人为制造DNA断裂。理论上所有细胞均应呈现强绿色。
目的:验证试剂盒是否有效。
结语
核心要点总结:"防止干片、温和操作、适度消化、全程避光"
防止干片:孵育过程务必保湿,可用防蒸发膜或塑料片覆盖;
温和操作:洗涤动作轻柔,离心收集易脱落的凋亡细胞;
适度消化:通透时间不宜过长,蛋白酶K使用需谨慎;
全程避光:从TUNEL反应开始直至观察结束,避免荧光淬灭。
TUNEL染色看似简单,但每一个细节都可能影响最终结果。希望这份指南能帮你避开那些"坑",做出漂亮、可靠的数据。
如果你有其他TUNEL染色的经验或问题,欢迎在评论区交流讨论~
关于晶莱
