

在慢性肾病(CKD)研究领域,单侧输尿管梗阻(UUO)模型是公认的研究肾间质纤维化的“金标准”。虽然原理看似简单——“扎住输尿管,等待纤维化”,但实际操作中,梗死程度不一、动物死亡率高、病理结果不典型等问题常常让新手科研人“破防”。
今天,小晶参考MCAO模型的严谨逻辑,为您奉上一份小鼠UUO模型不踩坑指南。
一、核心原理:为什么选UUO?
UUO模型通过结扎单侧输尿管,导致该侧肾脏尿液引流受阻,肾盂压力升高,进而引发肾小管扩张、间质炎症细胞浸润、成纤维细胞活化、细胞外基质沉积,最终形成肾间质纤维化。
该模型特点:
周期短:7-14天即可出现明显纤维化;
病变一致:纤维化程度与梗阻时间呈良好线性关系;
对侧对照:健侧肾脏可作为自身对照,减少个体差异。
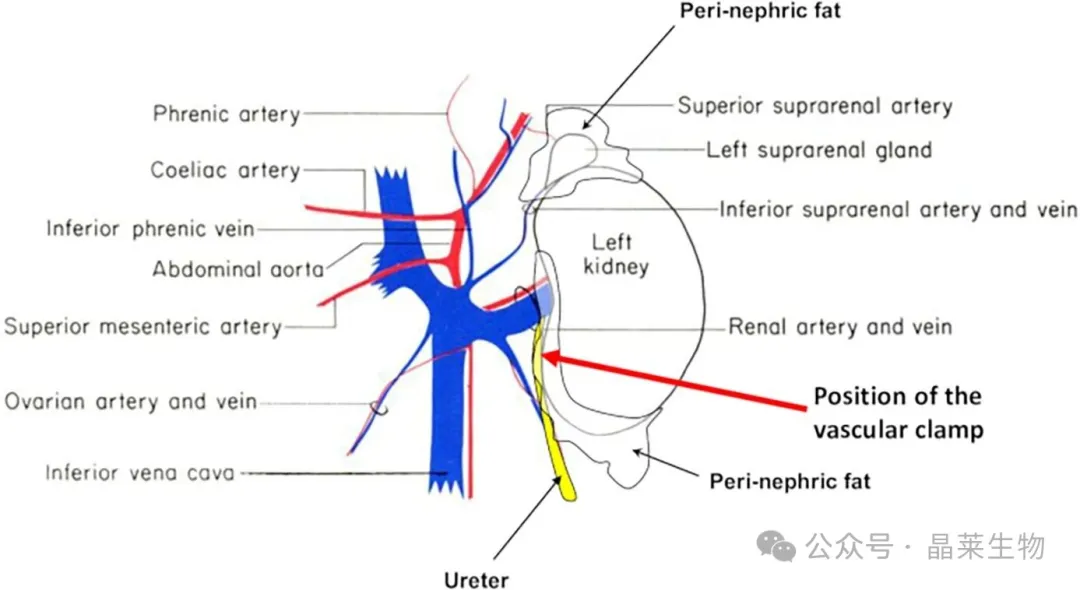
1. 术前准备:动物与器械
动物选择:
品系:C57BL/6小鼠优先(遗传背景清晰,纤维化反应稳定);
性别:雄性优先(避免雌激素对纤维化的干扰);
体重:20-25g(8-10周龄);
器械与耗材清单:
显微手术器械(眼科剪、显微镊、显微弯镊、持针器);
6-0丝线或5-0丝线(用于结扎输尿管);
手术显微镜(建议6-10倍放大);
恒温加热垫(维持肛温37±0.5℃);
缝线(5-0丝线用于缝合皮肤)。
2. 麻醉与固定
诱导:4-5%异氟烷(氧流量0.5-0.8L/min);
维持:1.5-2%异氟烷,面罩吸入。
小鼠左侧卧位固定,左侧腹部备皮;
碘伏消毒3遍,75%乙醇脱碘,铺无菌洞巾。
术中持续监测呼吸频率、皮肤颜色、趾反射;
加热垫维持体温,肛温探头监控。
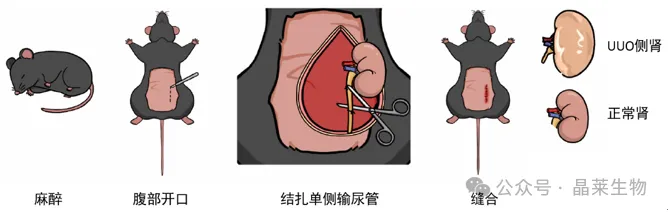
3. 手术操作分步图解(关键!)
第一步:暴露肾脏与输尿管
左侧腹部肋缘下0.5cm处做一纵向切口,长约1cm;
钝性分离皮下组织及肌肉层,暴露腹腔;
轻轻拉出左侧肾脏,沿肾门向下追踪输尿管。
第二步:分离输尿管
在显微镜下,用显微镊钝性分离输尿管周围结缔组织;
游离输尿管中上段约1cm长度,避免牵拉过度;
在输尿管下方穿一根6-0丝线备用。
第三步:结扎输尿管
在输尿管中段位置,用丝线打两个结,间距约2-3mm;
在两结之间剪断输尿管,确保完全阻断尿液引流;
观察近端输尿管是否迅速扩张,确认结扎成功。
第四步:关闭腹腔
将肾脏轻柔归位,避免扭转;
肌肉层用5-0丝线连续缝合,皮肤用3-0丝线间断缝合;
碘伏消毒切口,停麻醉。
4. 术后护理:决定生死的关键24h
即刻护理与观察指标:
将小鼠置于37℃恒温加热垫,侧卧位,保持气道通畅;
皮下注射生理盐水1ml补液;
单笼饲养,避免撕咬。
苏醒时间(一般5-10分钟);
术后1h、6h、24h观察精神状态、活动度、饮水情况;
若出现呼吸困难、持续抽搐、濒死状态,立即安乐死。
术中现象 | 可能原因 | 现场处理 |
输尿管难以分离 | 周围脂肪组织过多 / 误伤输尿管 | 镜下仔细辨认,避免牵拉,必要时从肾门向膀胱方向追踪 |
结扎后肾脏无扩张 | 结扎不彻底 / 误扎其他组织 | 重新分离,确保输尿管完全阻断 |
术后24h死亡 | 麻醉过深 / 失血过多 / 感染 | 控制麻醉深度,加强无菌操作,术后保温补液 |
纤维化程度差异大 | 梗阻时间不一致 / 结扎位置不当 | 统一结扎位置与时间,术后分组明确时间点 |
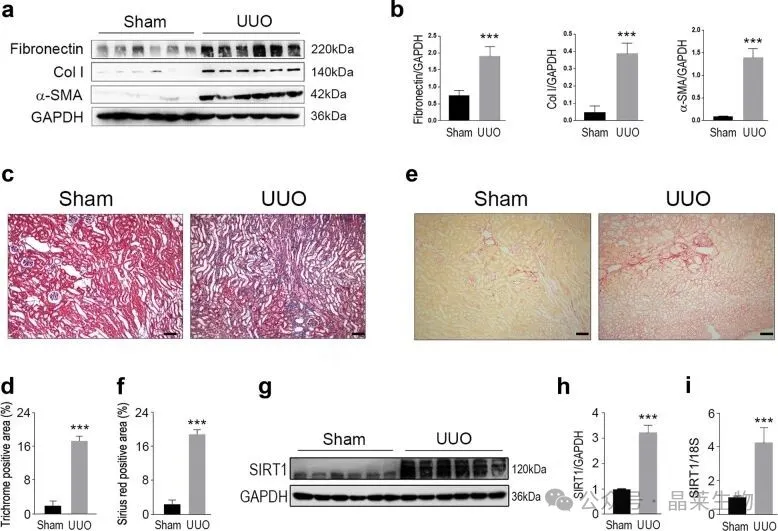
光凭手感不够,必须用客观的影像学和功能学指标验证模型成功与否。以下是目前顶刊通用的多模态验证方案。
1. 组织学染色(金标准)
HE染色:观察肾小管扩张、萎缩、间质增宽、炎症细胞浸润;
Masson染色:评估胶原纤维沉积程度,量化纤维化面积;
天狼星红染色:在偏振光下区分I型和III型胶原,敏感性更高。
避坑提示:切片厚度统一为3-5μm,染色时间标准化,避免批次间差异。
2. 免疫组化/免疫荧光(常用标志物)
α-SMA:肌成纤维细胞活化标志;
Collagen I/III:细胞外基质沉积;
F4/80:巨噬细胞浸润程度;
E-cadherin:肾小管上皮-间质转化(EMT)评估。
避坑提示:一抗孵育条件、抗原修复方式必须一致,确保定量可重复。
3. 分子生物学检测
Western Blot:检测纤维化相关蛋白(α-SMA、TGF-β1、Collagen I)表达;
qPCR:检测纤维化相关基因(TGF-β1, Col1a1, Col3a1, Fibronectin)表达;
ELISA:检测尿或组织裂解液中炎症因子(IL-1β, TNF-α, MCP-1)水平。
4. 肾功能与生化指标
血清肌酐(Cr)、尿素氮(BUN)可评估肾功能损害程度;
尿蛋白/肌酐比值(UPCR)反映肾小球功能。
注意:UUO模型为单侧梗阻,对侧肾脏代偿,血清肾功能指标变化不显著,建议结合组织学共同评估。
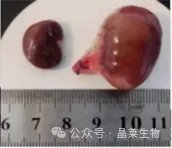
图4:假手术组(左)和UUO模型组(右)的肾脏对比图
验证层级 | 检测手段 | 核心指标 | 时间点 |
组织病理 | Masson/天狼星红 | 胶原沉积面积 | 术后7d、14d |
细胞活化 | IHC(α-SMA) | 肌成纤维细胞数量 | 术后7d、14d |
炎症反应 | IHC(F4/80) | 巨噬细胞浸润 | 术后3d、7d |
分子水平 | WB/qPCR | TGF-β1、Collagen I表达 | 术后7d、14d |
肾功能 | 血清Cr/BUN | 肾功能损害 | 术后14d |
只有将以上多模态数据整合起来,才能构建一个“病理-分子-功能”完整的证据链,让你的UUO模型数据真正达到顶刊水平。
1.结扎位置准、阻断彻底——模型成立的物理基础;
2.术中精细、术后护理——动物存活的保障;
3.多模态验证、数据闭环——文章发表的底气。
避开这些坑,你的UUO模型也能从“扎不准”到“稳扎稳打”。
结语
构建UUO模型,需要的不只是耐心,还有丰富的经验和标准化的流程。
【晶莱生物】拥有十年动物模型构建经验,深度掌握 300+ 种模型技术,覆盖神经、代谢、肿瘤、心血管等热门领域。
在UUO模型方面,我们已成功构建 1000+ 例,经验证:
模型成功率 >90%
术后7d存活率 >95%
纤维化面积标准差 <10%
我们配备全套组织病理平台、分子生物学平台及多模态成像系统,可提供从造模到多模态验证的一站式服务,让你的UUO实验不再“踩坑”。
关于晶莱
以上部分数据与结果图来源于网络和文献,如有侵权请联系客服删除。
[1] Delagado RD, de Caestecker MP. A Mouse Model to Evaluate the Long-Term Structural and Functional Outcomes after the Reversal of Prolonged Unilateral Ureteric Obstruction[J]. J VisExp, 2025(221): 10.3791/68492. DOI: 10.3791/68492.
[2] Li P, Liu Y, Qin X, et al. SIRT1 attenuates renal fibrosis by repressing HIF-2α[J]. Cell Death Discovery, 2021, 7(1): 59. DOI: 10.1038/s41420-021-00443-x.
[3] Understanding Animal Research. Black laboratory mouse in purple gloved hand[EB/OL]. Wikimedia Commons,许可协议:CC BY-SA 4.0
[4] Shvets A. Clos-up of Surgical Instruments[EB/OL]. Pexels, 2021