

本文献研究首次建立可长期扩增且保留完整代谢功能的人成体肝细胞类器官(HHO),通过Wnt+STAT3双通路激活(关键因子为抑瘤素M,OSM)解决了体外肝细胞“扩增就丢失功能、保功能就无法扩增”的trade-off难题。OSM既能强力驱动增殖,又能阻止胆管化生,维持肝细胞身份。该类器官可在小鼠肝脏内定植重建、形成代谢分区,并完整复现胆汁酸合成、脂质代谢、药物代谢、糖异生、尿素循环等全部核心肝功能;同时支持高效基因编辑,可构建糖原贮积病、尿素循环障碍等代谢肝病模型。该体系为肝病机制研究、药物筛选、细胞治疗提供了突破性功能工具。

本研究优化了类器官培养条件,实现了人原代肝细胞的长期扩增与定向成熟分化。所构建的肝细胞类器官无导管化生表型,且展现出与人原代肝细胞相当的代谢功能。对肝细胞代谢的精准体外模拟,开启了功能性类器官医学的新时代。
1. 核心研究:
①依据肝癌基因组(TCGA)筛选关键通路:WNT、STAT3、TGFβ、PKA、RAS。
②建立扩增培养基(EM):含EHF(EGF+HGF+FGF10)、Wnt/R-spondin、TGFβ抑制剂、Noggin、forskolin。
③成功从成人原代肝细胞(PHH)长出厚壁、高表达ALB/HNF4α的肝细胞类器官(HHO),排除胆管类器官(ICO)干扰。实现长期稳定传代(≥3个月),基因组保持稳定。
2. 经限定因子诱导的人成体肝细胞类器官扩增
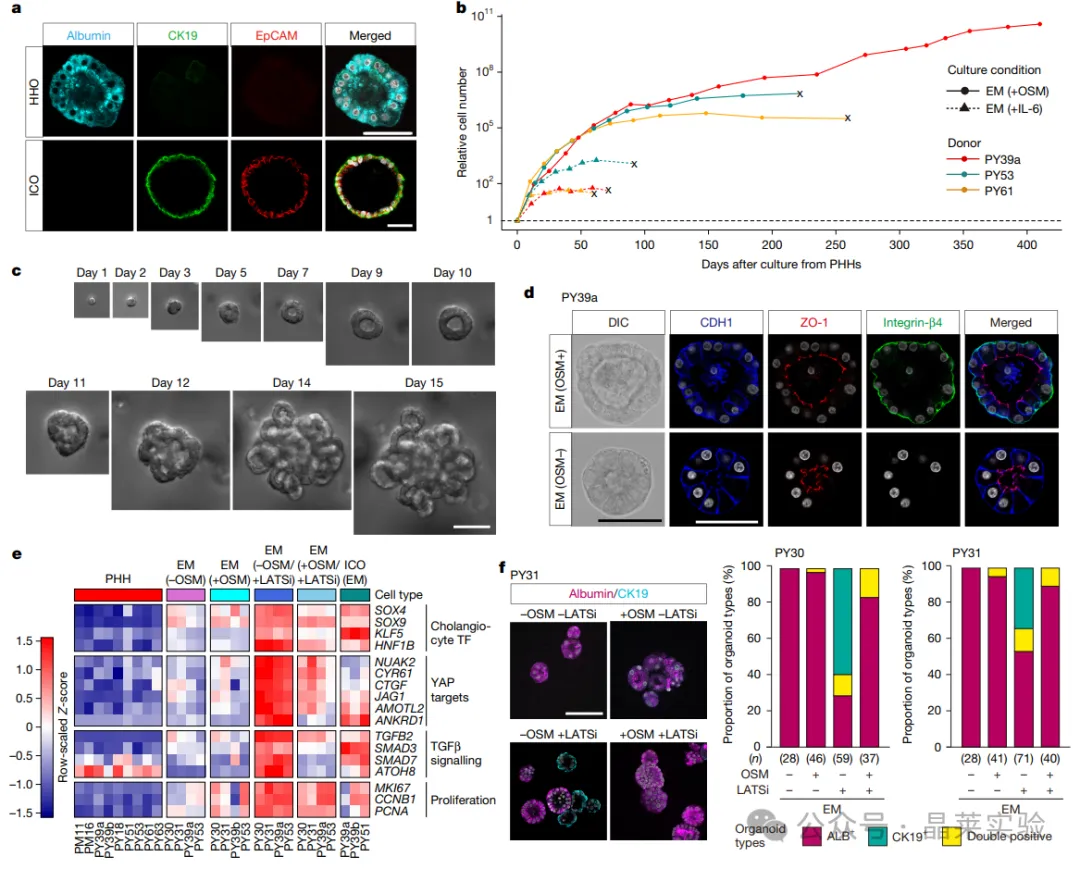
a.扩增培养基(expansionmedium,EM)(+IL-6)中培养的原代肝细胞来源类器官的免疫荧光染色结果。人肝细胞类器官(HHOs)表达白蛋白,而肝内胆管细胞类器官(ICOs)表达CK19和EpCAM。细胞核采用Hoechst33342染色。3例供体样本均获得了相似结果。
b.含OSM或IL-6的扩增培养基中,原代肝细胞来源人肝细胞类器官的扩增情况。细胞数通过传代比例和基于ATP的细胞计数进行估算。每个点代表一次传代操作。3个类器官细胞系在最初3个月内,约每2周传代一次,传代比例为1:3~1:12;“x”代表传代失败。PY39a、PY53、PY61分别代表39岁、53岁、61岁的供体。
c.单个原代肝细胞在OSM诱导下类器官生长的延时成像图。同一类器官在相同放大倍数下拍摄。2例供体样本均获得了相似结果。
d.OSM对人肝细胞类器官基底极性的影响。代表性明场图像和全组织免疫染色结果:CDH1(蓝色)、ZO-1(红色)、整合素β4(绿色)、细胞核(白色)。4例供体样本均获得了相似结果。定量结果见扩展数据图3a。
e.原代肝细胞、肝内胆管细胞类器官,以及添加/不添加OSM和LATS抑制剂(LATSi,TRULI,5μM)处理的人肝细胞类器官中,胆管细胞相关转录因子、YAP靶基因及TGFβ信号相关基因的转录组分析结果。PM11和PM16分别代表11月龄和16月龄的供体。
f.添加/不添加OSM和LATS抑制剂(5μM)培养14天的人肝细胞类器官。左图为白蛋白(Alb)和CK19的免疫染色结果,细胞核采用Hoechst33342染色。右图为2例供体来源类器官免疫表型的占比统计,2例样本结果相似。仅在无OSM、添加LATS抑制剂的条件下,可观察到CK19阳性类器官。
3. 抑瘤素M(OSM)调控人肝细胞类器官的生长与极性
①OSM是最强扩增因子:通过激活STAT3实现指数级增殖,远优于IL-6。
②决定基底极性:上调integrinβ4等黏附分子,让类器官形成上皮样囊状结构,利于与基质胶黏附生长。
③分选BSC-low肝细胞可提高类器官形成率,提示BSC可反映解离应激程度。
④单细胞也能形成类器官,不受年龄与贴壁能力限制。
4. OSM阻断人肝细胞类器官的胆管谱系分化
①YAP激活促增殖但诱导胆管化生:LATS抑制剂(LATSi)激活YAP会让肝细胞转成胆管表型(CK19、SOX9、SOX4上调)。
②OSM完全拮抗胆管化生与EMT:抑制YAP/TGFβ靶基因,维持肝细胞身份。
③机制:OSM–STAT3独立于YAP驱动增殖,两者可协同扩增,但只有OSM能保留肝细胞特性。
1.人肝细胞类器官的分区特异性分化
①建立分化培养基(DM):撤去OSM/Wnt/Noggin,加激素+DAPT。
②可定向分化为:门静脉区(PV)型dHHO;中央静脉区(CV)型dHHO+WR(补回Wnt/R-spondin)。
③饥饿处理是代谢成熟必需条件;转录谱高度接近原代肝细胞。
2.人肝细胞类器官中的脂质代谢
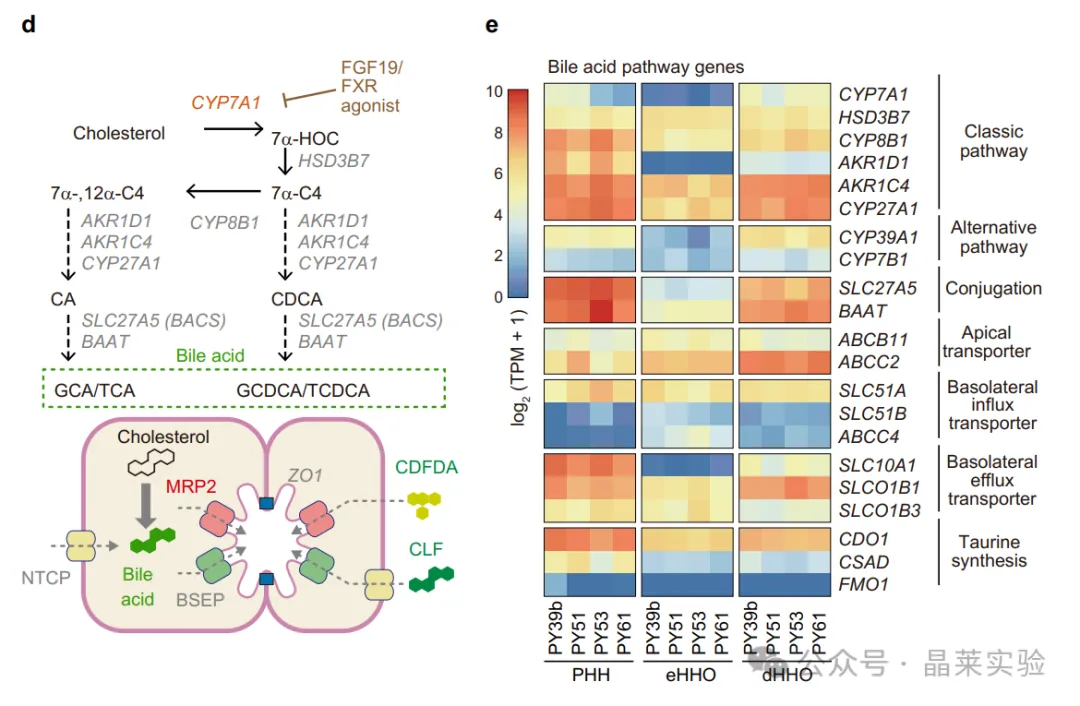
①分化后形成完整胆小管网络,具备BSEP/MRP2转运功能。
②高表达CYP7A1等限速酶,合成与人一致的结合型胆汁酸。
③可合成甘油三酯,形成脂滴,能模拟脂肪肝(steatosis)。
④可被FXR/FGF19负反馈调控,适用于脂代谢药物筛选。
3.人肝细胞类器官中的药物代谢
①高表达CYP3A4、CYP2E1、CYP1A2等关键药酶。
②具备基础活性+药物诱导活性(利福平、苯巴比妥、奥美拉唑)。
③能精准重现对乙酰氨基酚(APAP)肝毒性,灵敏度远高于传统模型。
④保留Ⅱ相结合反应,是理想的药物代谢与毒理模型。
4.具备代谢功能的分化型人肝细胞类器官(dHHOs)的构建
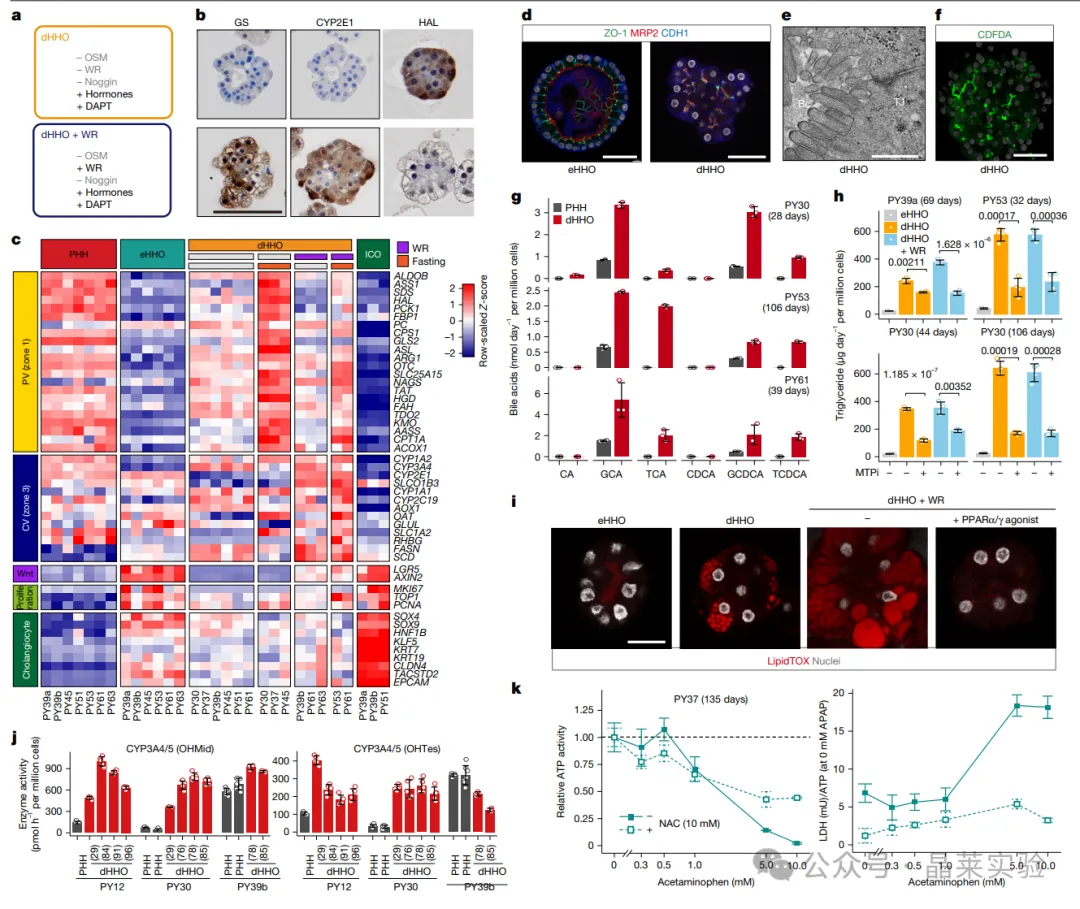
a.门静脉(PV)型分化类器官(dHHO)和中央静脉(CV)型分化类器官(dHHO+WR)的分化培养条件。
b.分化型人肝细胞类器官(上图)和dHHO+WR组类器官(下图)的分区标志物染色代表性图像,分化型人肝细胞类器官经饥饿处理后染色。3例供体样本均获得了相似结果。
c.转录组测序(RNA-seq)数据集中,原代肝细胞、扩增型人肝细胞类器官、添加/不添加WR和饥饿处理的分化型人肝细胞类器官,以及胆管细胞类器官中,中央静脉、门静脉、Wnt靶基因、增殖相关及胆管细胞标志物基因的表达情况。
d.扩增型和分化型人肝细胞类器官中ZO-1(绿色)、MRP2(红色)、CDH1(蓝色)的免疫染色结果(另见扩展数据图7a)。3例供体样本均获得了相似结果。
e.分化型人肝细胞类器官的透射电镜图像,可见紧密连接(TJ)和胆小管(Bc)。2次生物学重复中,至少观察30个类器官,均获得了相似结果。
f.分化型人肝细胞类器官中,MRP2介导的CDFDA外排的3D重建图像。5例供体样本均获得了相似结果。
g.原代肝细胞和分化型人肝细胞类器官培养上清中的胆汁酸含量。每个点代表1个复孔,数据为均值±标准差,3例供体。CA:胆酸;GCA:甘氨胆酸;TCA:牛磺胆酸;GCDCA:鹅脱氧胆酸;GCDCA:甘氨鹅脱氧胆酸;TCDCA:牛磺鹅脱氧胆酸。
h.经MTP抑制剂(MTPi,1μM)处理/不处理的人肝细胞类器官的甘油三酯生成量。3例供体,PY30样本在2个不同时间点检测。每个点代表1个技术重复,每组4个复孔,数据为均值±标准差。采用Welch双侧t检验。
i.扩增型人肝细胞类器官、分化型人肝细胞类器官、dHHO+WR组类器官的代表性LipidTOX染色结果。PPARα/γ激动剂(WY-14643,100μM)可降低脂质合成。2个类器官细胞系在2个不同时间点均获得了相似结果。定量结果见扩展数据图7h。
j.原代肝细胞和分化型人肝细胞类器官的基础CYP酶活性。实验流程见扩展数据图8b。3例供体在不同时间点检测,每个点代表1次实验重复。分化型人肝细胞类器官在2D铺板前,按标注时长进行培养。误差线为均值±标准差:PY12(原代肝细胞n=5,分化型类器官n=5,4个条件)、PY30(原代肝细胞n=8,分化型类器官n=5,4个条件)、PY39b(原代肝细胞n=7,2次重复;分化型类器官n=3,2个条件)。其他CYP酶活性结果见扩展数据图8c。
k.对乙酰氨基酚处理后,分化型人肝细胞类器官的剂量-反应曲线,通过ATP活性(细胞活力)和乳酸脱氢酶(LDH)释放(细胞损伤)检测。额外2次重复结果见扩展数据图8g。数据为每个时间点3个技术重复的均值±标准差,3例供体样本均获得了相似结果(另见扩展数据图8g)。
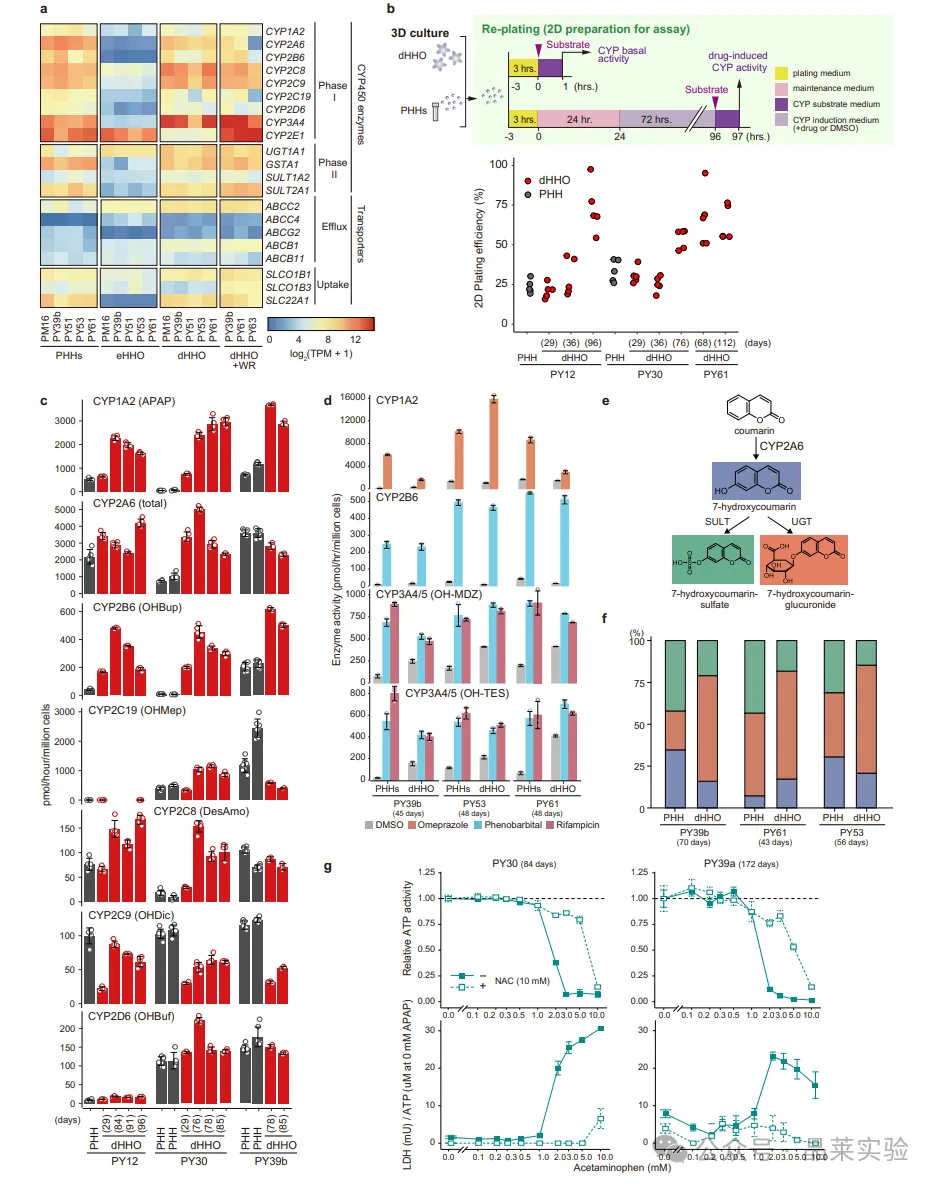
图 8 人肝细胞类器官中的药物代谢
基因敲除人肝细胞类器官的构建
1. 基因敲除人肝细胞类器官的构建
①突破瓶颈:LATSi+人血小板裂解物让基因编辑后不停止生长、不发生胆管化生。
②成功构建G6PC敲除(糖原贮积病)和OTC敲除(尿素循环障碍)模型。
③功能验证:G6PC-KO:糖异生下降OTC-KO:无法合成瓜氨酸、尿素合成障碍,可用于遗传性代谢肝病精准建模。
2.基因敲除肝细胞类器官的构建
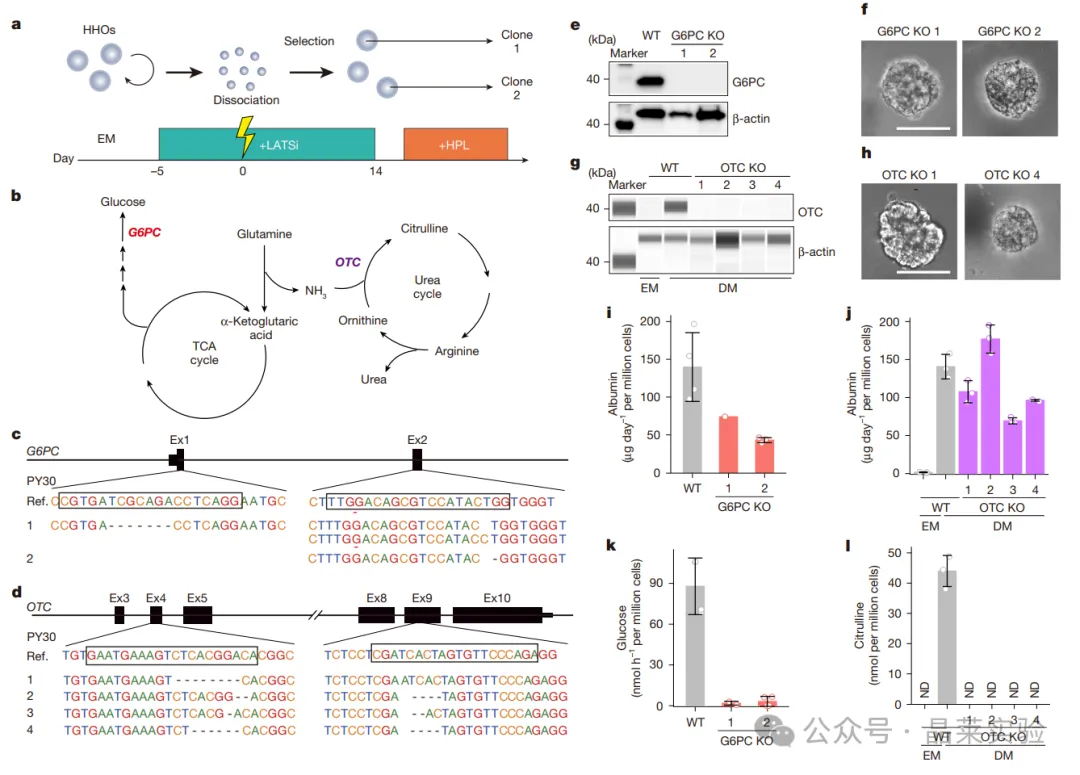
a.基因编辑人肝细胞类器官的构建流程。
b.糖异生和尿素循环通路示意图,加粗标注了选择敲除的基因。
c~h.基因敲除人肝细胞类器官的构建验证。c、d:分别采用2种和3种不同sgRNA构建的G6PC(c)和OTC(d)敲除类器官的Sanger测序验证结果。e、g:G6PC(e)和OTC(g)敲除类器官的蛋白水平验证结果。f、h:G6PC(f)和OTC(h)敲除类器官的形态学观察结果。
i、k.野生型(WT)和G6PC敲除人肝细胞类器官的白蛋白(i)和葡萄糖(k)生成量。
j、l.野生型和OTC敲除人肝细胞类器官的白蛋白(j)和瓜氨酸(l)生成量。
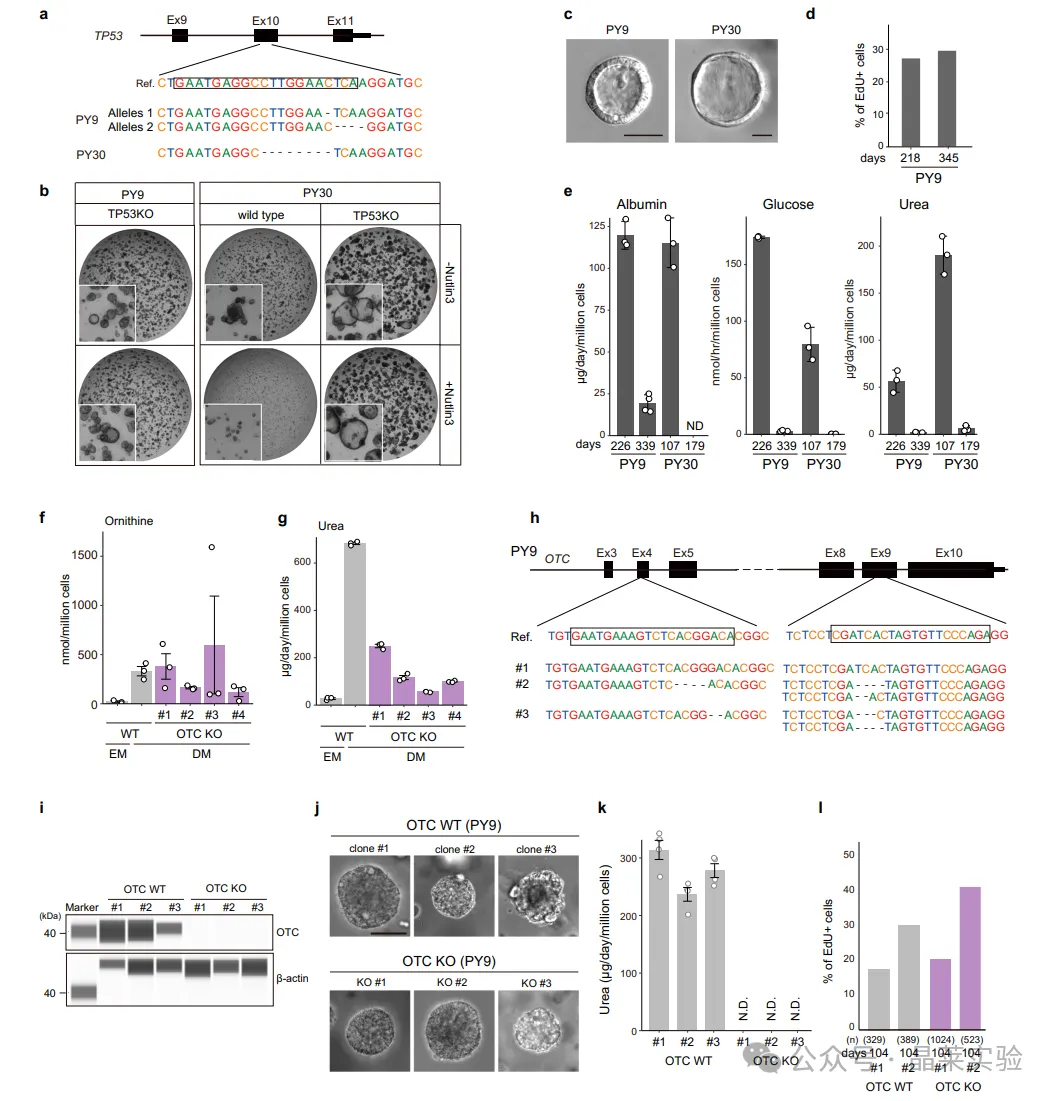
a.Sanger测序证实2例不同供体(PY9和PY30)来源类器官中TP53的敲除,构建了2个敲除克隆。
b.MDM2抑制剂Nutlin-3处理对TP53敲除类器官的筛选结果。比例尺:500μm。至少3次技术重复均获得了相似结果。
c.TP53敲除人肝细胞类器官的代表性形态,可见导管样囊状结构。比例尺:100μm。观察至少50个类器官,均获得了一致结果。
d.TP53敲除人肝细胞类器官的EdU阳性细胞百分比。底部标注了原代肝细胞来源后的培养天数,分别分析了218天(n=47)和345天(n=73)的细胞。
e.TP53敲除人肝细胞类器官的白蛋白分泌、葡萄糖生成和尿素合成能力。底部标注了原代肝细胞来源后的培养天数,数据来自2个TP53敲除克隆,每个点代表1个复孔,数据和误差线为3个技术重复的均值±标准差。
f、g.野生型(WT)和OTC敲除人肝细胞类器官的鸟氨酸(f)和尿素(g)生成量。每个点代表1个复孔,数据和误差线为3个技术重复的均值±标准差。
h~j.额外OTC敲除人肝细胞类器官的构建。h:Sanger测序证实PY9供体来源类器官中OTC的额外敲除,构建了3个敲除克隆;同时导入GFP表达载体作为对照,构建了3个GFP表达克隆。i:OTC野生型和敲除克隆中OTC敲除的蛋白水平验证。j:GFP表达的野生型克隆和OTC敲除人肝细胞类器官的形态学观察。每个克隆至少观察50个类器官,均获得了一致结果。
k.与野生型人肝细胞类器官克隆相比,OTC敲除人肝细胞类器官的尿素合成能力。类器官在无精氨酸、含1mM鸟氨酸的糖异生检测培养基中培养。每个点代表1个复孔,数据和误差线为4个技术重复的均值±标准差。
l.野生型GFP克隆和OTC敲除人肝细胞类器官的EdU阳性细胞百分比。底部标注了原代肝细胞来源后的培养天数,n代表每个克隆类器官细胞系中分析的细胞数。
关于晶莱