

基于类器官技术构建的肝脏与胰腺模型,为胚胎发育、器官功能、疾病建模及临床应用相关基础科学问题的研究,提供了可及性高、以人源体系为主的研究平台。
肝胰类器官可通过多种起始材料构建,包括多能干细胞、胚胎 / 胎儿 / 成体干细胞,以及成体分化细胞,各类起始材料均具备其特有的优势与局限性。
现有肝胰类器官模型,已帮助研究者深入解析了体内模型无法实现的获得性与先天性疾病的相关机制。
两类器官都可从多能干细胞(PSC)与组织驻留细胞两大来源构建,是少数同时支持两种来源的器官。
核心差异
肝脏:更容易获得功能性肝细胞类器官,可直接来自成人肝细胞;更易做代谢/胆汁/纤维化模型。
胰腺:内分泌(胰岛/β细胞)更难成熟;成体主要以导管类器官为主,是PDAC胰腺癌建模主力。
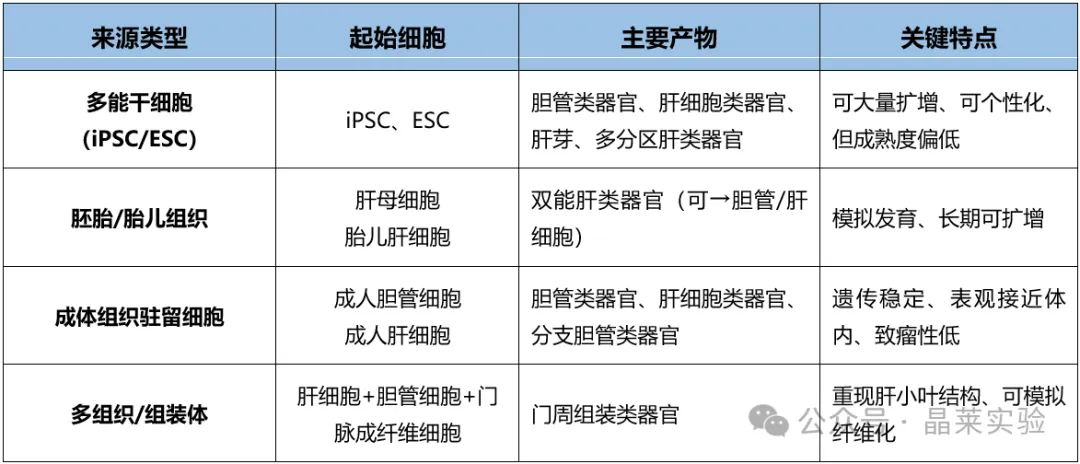
源自不同组织驻留细胞的肝脏类器官
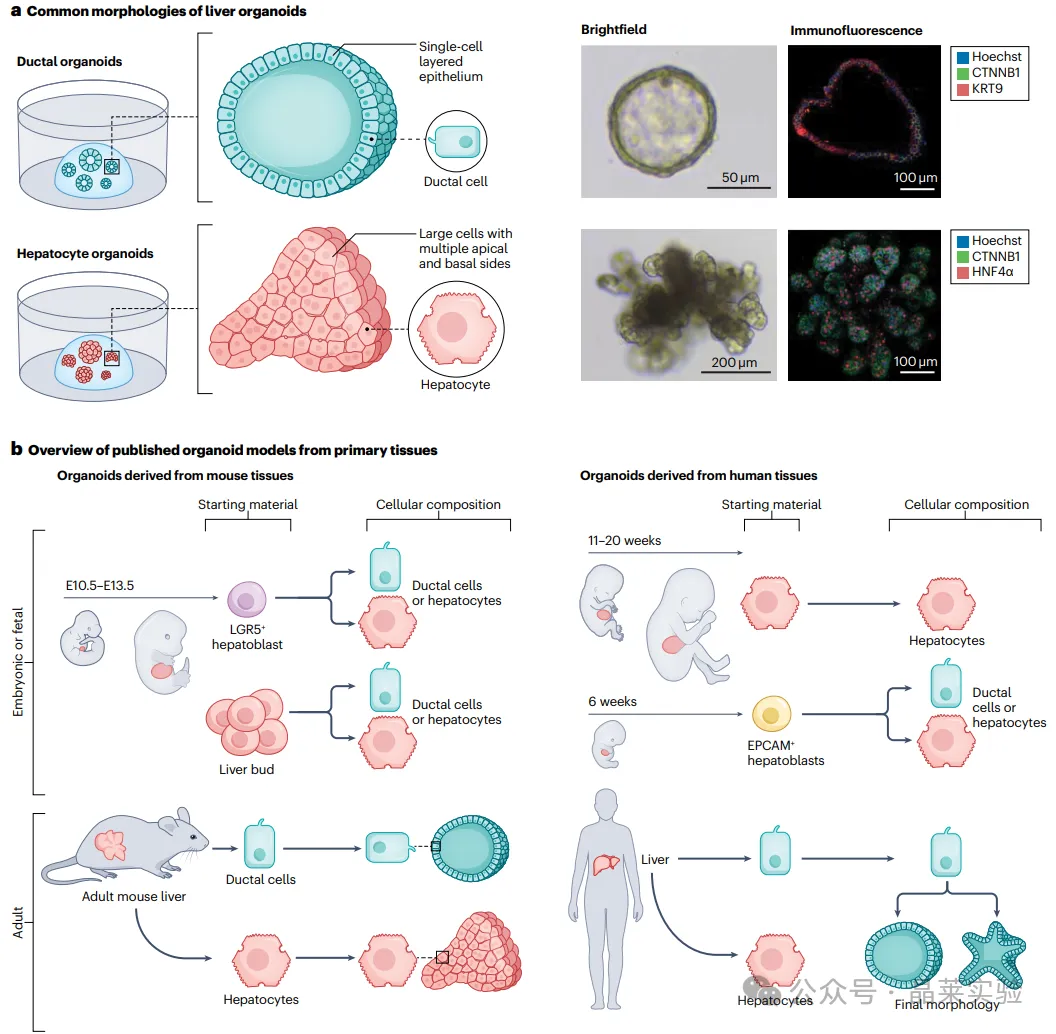
a. 肝导管细胞(左上图)与肝细胞(左下图)来源的肝脏类器官的常见形态。导管细胞可形成具有典型囊状管腔的单层上皮类器官,而肝细胞类器官则形成致密的分支状结构。右侧显微图像展示了肝母细胞来源的小鼠类器官;肝母细胞是胚胎期的双能祖细胞,可根据所用培养基的差异,诱导培养为导管样或肝细胞样类器官。明场成像下,导管类器官呈囊状结构(上图),肝细胞类器官则表现为不透明结构(下图)。免疫荧光图像分别展示了特征性上皮标志物(CTNNB1,β- 连环蛋白)、导管细胞特异性标志物 KRT19、肝细胞特异性标志物 HNF4α 的表达情况。
b. 已发表的部分原代肝上皮细胞来源类器官模型的研究概况。左侧为小鼠细胞来源的类器官,右侧为人源细胞来源的类器官;上方为发育期肝脏来源的类器官,下方为成年期肝脏(小鼠,8~12 周龄)来源的类器官。导管类器官可由原代导管细胞诱导构建,肝细胞类器官可由原代肝细胞诱导构建。此外,肝细胞类器官与导管类器官均可由单一细胞来源 —— 胚胎肝母细胞诱导构建。
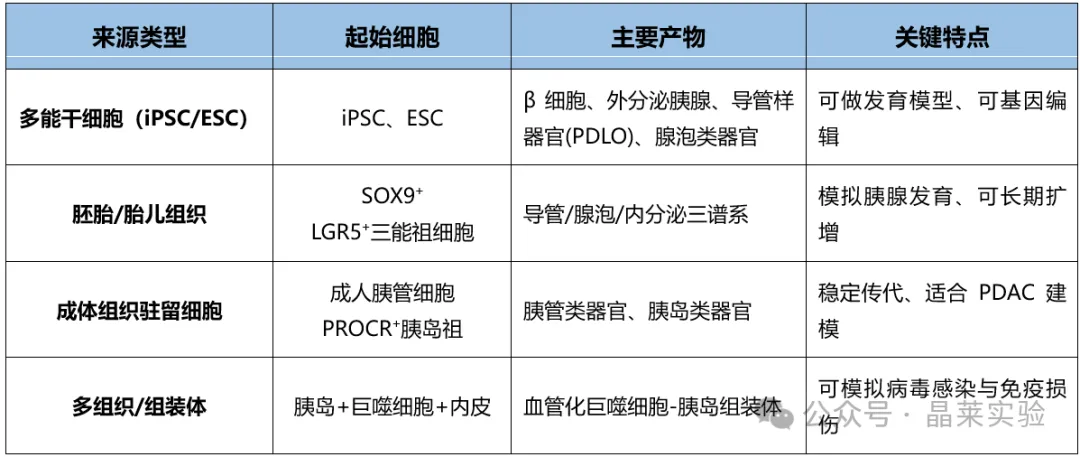
源自不同组织驻留细胞的胰腺类器官
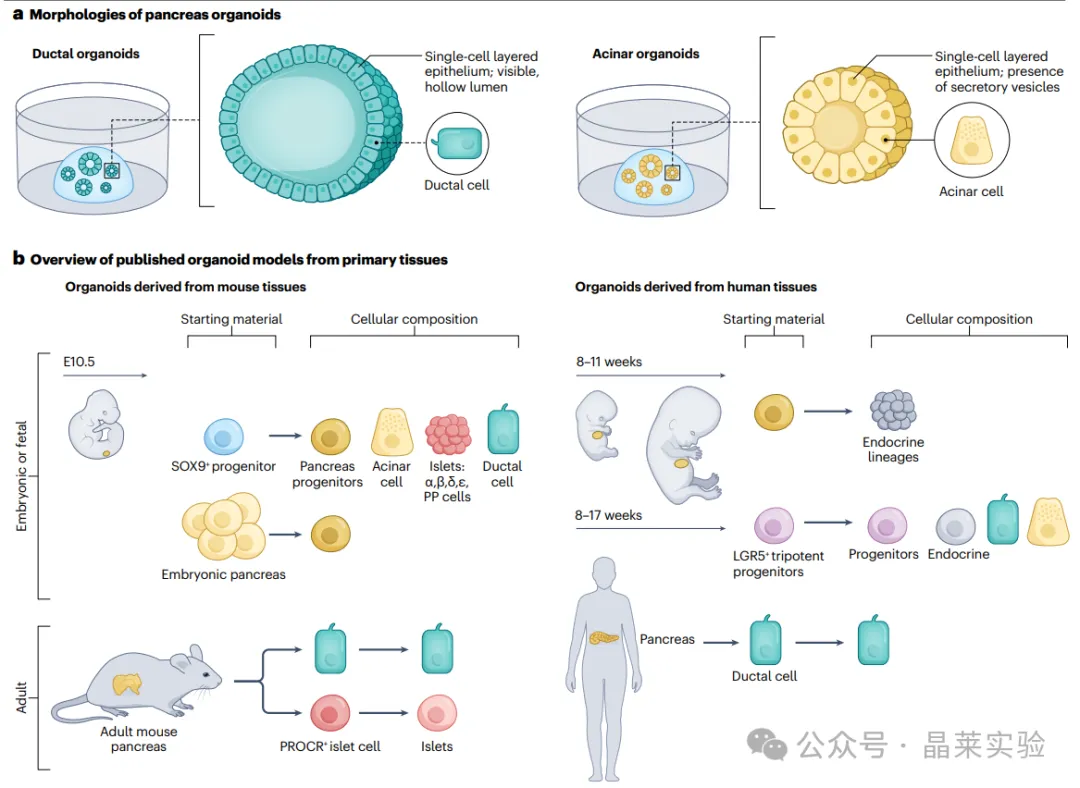
b. 已发表的部分原代胰腺细胞来源类器官模型的研究概况。左侧为小鼠细胞来源的类器官,右侧为人源细胞来源的类器官;上方为发育期胰腺来源的类器官,下方为成年期胰腺来源的类器官。
1. 基于肝脏类器官的疾病模型构建
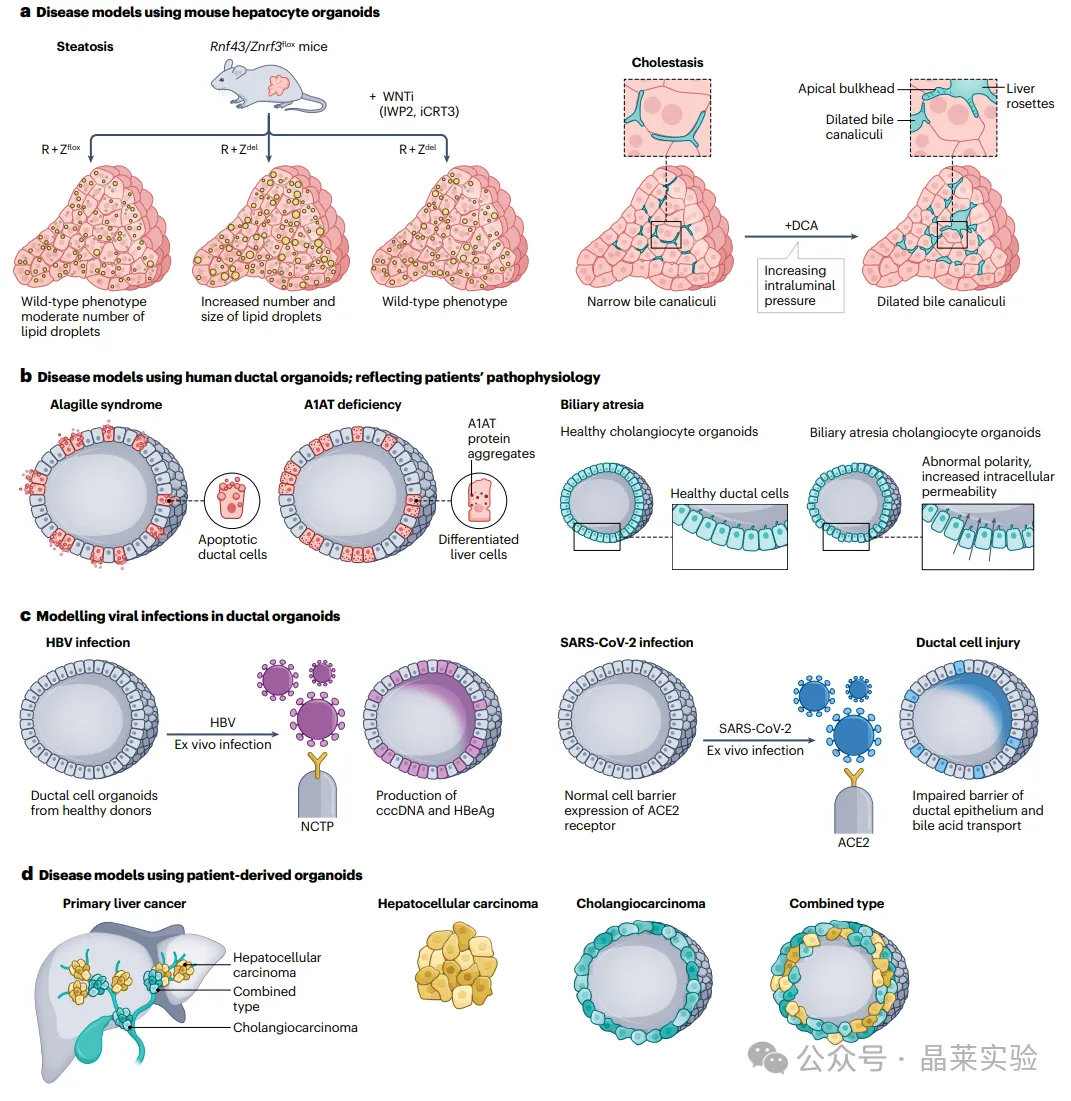
肝脏类器官可用于疾病相关病理特征的模型构建:既可以患者细胞(图 b)或健康细胞为起始材料构建类器官,也可用于模拟小分子给药(图 a)或病毒感染(图 c)后的疾病应答。此外,可通过患者组织构建类器官,用于多种肿瘤的模型构建;所得肿瘤类器官可完整重现原发肿瘤的遗传学特征与表型特征(图 d)。
2.先天性遗传病
①α1-抗胰蛋白酶缺乏症:蛋白聚集表型;
②Alagille综合征:胆管细胞凋亡、胆管减少;
③多囊肝病:可用于全基因组测序;
④糖原贮积病1a型(GSD1a):脂质/糖原蓄积;
⑤囊性纤维化(CFTR突变):胆管功能异常。
3.代谢与脂肪性肝病(MASLD/NASH)
①游离脂肪酸诱导或CRISPR编辑(PNPLA3ⁱ¹⁴⁸ᵐ、APOB/MTTP敲除)造模,可用于筛选ACC、FAS、DGAT2等抑制剂可减少脂滴,揭示WNT通路(RNF43/ZNRF3)调控脂肪变性。
4.胆汁淤积&胆管病
①Mdr2⁻/⁻肝细胞类器官:重现遗传性胆汁淤积;
②脱氧胆酸诱导:急性胆汁淤积、胆小管扩张;
③胆道闭锁:上皮发育延迟、屏障受损;
④原发性硬化性胆管炎:胆汁来源类器官可复现炎症表型。
5.感染模型
①HBV感染:建立cccDNA复制、癌前基因特征;
②SARS-CoV-2:直接感染胆管上皮、导致肝损伤。
6.肝癌模型(HCC/胆管癌/混合型)
患者肿瘤类器官保留原发突变与药物谱,用于个体化药敏、ERK抑制剂、索拉非尼测试
7.临床应用
①药物肝毒性筛选;
②基因治疗与CRISPR修复;
③移植修复肝损伤(肝芽、多分区肝类器官)。1.基于胰腺类器官的疾病模型构建
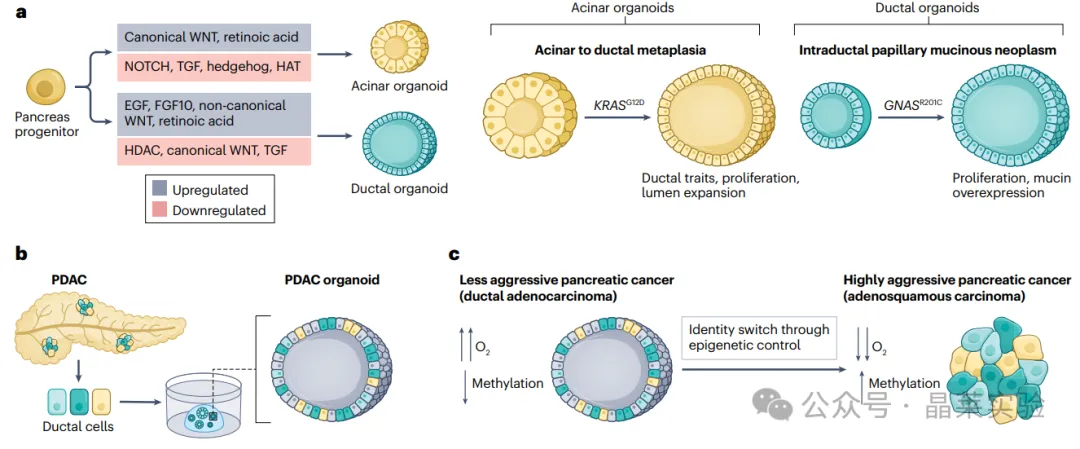
胰腺类器官目前主要应用于胰腺癌的模型构建与相关研究。可通过向健康的腺泡或导管类器官中引入突变,构建胰腺癌类器官(图 a)。此外,可通过患者活检样本构建类器官,用于胰腺导管腺癌(PDAC)的模型构建;所得 PDAC 类器官可完整重现原发肿瘤的遗传学特征与表型特征(图 b)。肿瘤类器官还可用于揭示肿瘤微环境的改变,如何通过表观遗传调控驱动肿瘤向更高侵袭性的亚型进展(图 c)。
2.胰腺癌(PDAC,占85%)
①来源:患者手术/穿刺样本、iPSC祖细胞;
②突变研究:KRASᴳ¹²ᴰ促腺泡-导管化生;GNASᴿ²⁰¹ᶜ促导管囊性扩张;
③分型:WNT依赖型/非依赖型;鳞癌转化受TP63、缺氧、WNT缺乏调控;
④应用:个体化药物筛选、肿瘤异质性、靶向药开发.
3.先天性遗传病:囊性纤维化(CFTR):导管类器官对forskolin无肿胀,用于药物筛选
4.糖尿病(内分泌)
①iPSC→β细胞/胰岛类器官:葡萄糖刺激胰岛素分泌;
②PROCR⁺祖细胞来源胰岛类器官:可逆转小鼠1型糖尿病;
③临床:iPSC胰岛移植恢复患者胰岛素不依赖(2024临床)。
5.感染与免疫模型:血管化巨噬细胞-胰岛组装体:模拟病毒诱导β细胞焦亡。
6.临床应用
①糖尿病细胞替代治疗;
②胰腺癌精准用药;
③胰腺发育与再生机制研究。
1. 肝脏类器相关技术突破
①成人肝细胞类器官实现生理胆小管网络
Dowbajetal.2025(Nature)
首次在体外重建接近体内尺寸与连通性的胆小管网络;
可精准建模胆汁淤积、Mdr2缺陷、顶端隔板等病理结构;
构建门周组装类器官,重现肝小叶三维结构与纤维化。
② 人源多分区肝类器官(mZ-HLO)
AlRezaetal.2025(Nature)
iPSC构建分区1+分区3肝细胞联合类器官;移植后显著改善高氨血症、高胆红素血症,提高存活率。
③成人肝细胞高效扩增体系
Igarashietal.2025;Yuanetal.2025
WNT+STAT3或YAP激活,实现人原代肝细胞长期扩增;保留代谢、解毒、胆小管功能。
2.胰腺类器官相关技术突破
①人胎儿LGR5⁺三能胰腺干细胞
Andersson-Rolfetal.2025(Cell)
单个细胞可长期扩增并产生导管、腺泡、内分泌三谱系;仅存在于人胎儿期,为胰腺发育提供全新模型。
②分支胰腺类器官
Darrigrandetal.2025
2D+微孔板+悬浮培养,获得空间分区的胰腺分支结构;更贴近体内胰腺形态,用于研究形态发生与癌变。
3.共性技术突破(肝+胰)
①化学成分明确合成水凝胶:替代Matrigel,支持胰管/胆管类器官长期培养,向GMP临床级迈进。
②多谱系组装类器官(assembloids)标准化:实现上皮+间质+内皮共培养,大幅提升生理仿真度。
③单细胞图谱+基因编辑:系统解析导管/腺泡/肝细胞异质性,用于精准疾病建模。
关于晶莱