

核心定义与本质特征
患者来源类器官(PDOs)是从患者肿瘤组织(手术标本、穿刺活检、转移灶)或体液脱落细胞(如尿液)中分离肿瘤干细胞,在三维培养体系中自组织形成的类肿瘤结构。其核心本质是体外精准复刻患者原发肿瘤的遗传异质性、组织学结构、表型特征与功能特性,被称为"患者肿瘤的体外功能替身"。
泌尿生殖系统肿瘤患者来源类器官(PDOs)的构建与应用
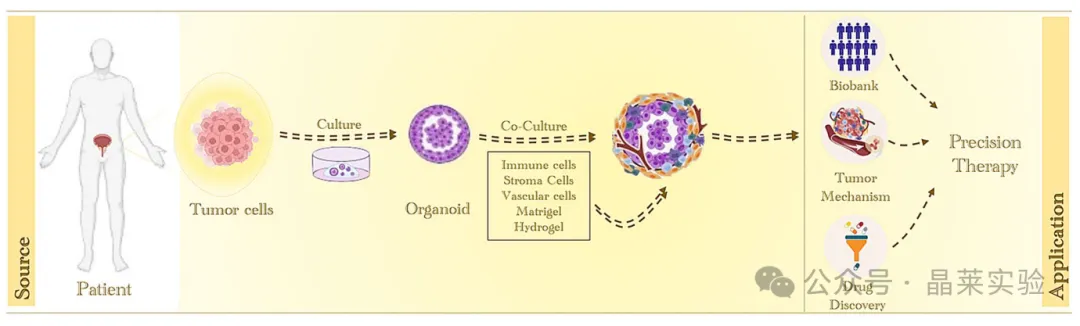
源自泌尿生殖系统肿瘤的患者来源类器官,在模拟天然肿瘤微环境的条件下进行构建与培养。此类模型可作为个性化药物筛选、生物标志物鉴定及机制研究的功能平台,旨在将患者特异性肿瘤生物学特征转化为个体化治疗策略。
泌尿生殖系统肿瘤(尤其是前列腺癌、肾癌、膀胱癌)因分子异质性与治疗耐药性,仍是临床主要挑战。
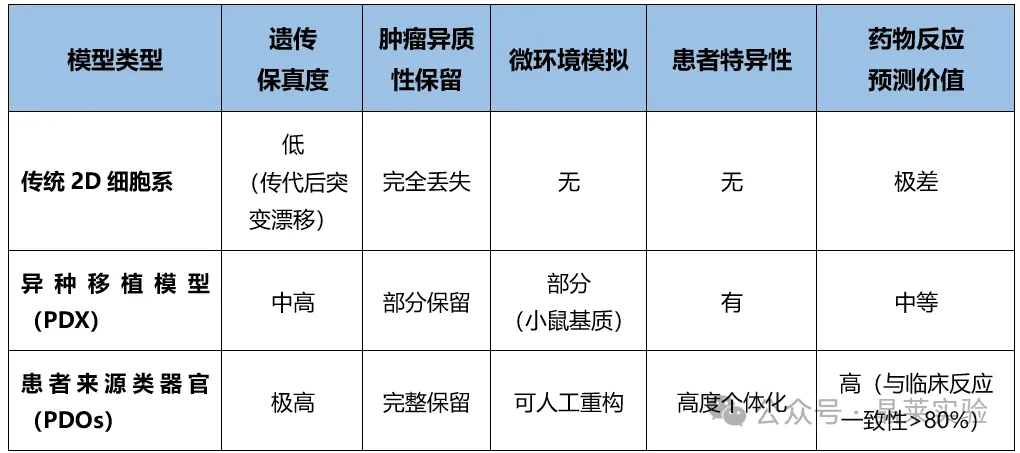
患者来源类器官(PDOs)可精准复刻个体肿瘤的遗传、表型与功能复杂性,预测价值优于传统二维培养或动物模型。
PDOs可实时评估药物敏感性、耐药机制与克隆进化,支持科研与临床场景的精准肿瘤学应用。
PDOs与液体活检(循环肿瘤DNA、循环肿瘤细胞、尿液生物标志物)整合,构建微创动态平台,监测肿瘤进化并动态调整治疗方案。
类器官生物样本库建设与生物信息学整合流程,是将PDOs打造为个体化肿瘤治疗功能替身的关键。

1.前列腺癌PDOs
①复刻所有疾病阶段,包括最难治疗的神经内分泌前列腺癌;
②能模拟AR通路的多种耐药机制:AR扩增/突变、AR剪接变体、旁路通路激活(PI3K/AKT、WNT);
③相关研究已成功用于验证PARP抑制剂在DNA修复缺陷(BRCA1/2、ATM)患者中的疗效。
2.膀胱癌PDOs
①生物样本库已覆盖所有主要分子亚型,药物反应与患者临床结局高度一致;
②携带FGFR3突变的类器官对厄达替尼等FGFR抑制剂表现出特异性敏感性;
③BCG耐药类器官模型揭示了细胞因子信号受损与干扰素通路异常的核心机制。
3.肾癌PDOs
①目前唯一能完整保留肾细胞癌瘤内异质性的体外模型;
②转移灶来源类器官与原发灶类器官的药物敏感性存在显著差异,提示转移灶需个体化治疗;
③免疫共培养模型可用于评估免疫检查点抑制剂疗效,为免疫治疗耐药患者提供新方案。
1.高通量药物筛选与耐药机制研究
①前列腺癌:筛选PARP抑制剂、PI3K/AKT抑制剂、新一代AR通路抑制剂;发现极光激酶抑制剂对神经内分泌亚型的治疗潜力;
②膀胱癌:测试化疗药物、FGFR抑制剂、免疫治疗药物;筛选BCG耐药患者的替代膀胱内治疗方案(溶瘤病毒、STING激动剂);
③肾癌:评估VEGFR抑制剂、HIF-2α抑制剂、mTOR抑制剂及ICI-TKI联合方案;发现代谢与表观遗传靶向的新治疗靶点。
2.肿瘤生物学机制研究
①解析肿瘤克隆进化与治疗选择压力下的适应性改变;
②研究肿瘤-微环境互作(成纤维细胞、免疫细胞、细胞外基质)对治疗反应的影响;
③揭示激素交叉调控(雄激素-甲状腺激素)、代谢重编程、免疫逃逸等关键生物学过程;
④利用CRISPR/Cas9基因编辑技术验证特定驱动基因的功能。
3.个体化精准治疗指导
①为晚期耐药患者筛选最有效的个体化治疗方案,避免无效治疗;
②预测患者对特定药物的反应,实现"先试药后用药";
③为罕见亚型或难治性患者提供治疗选择依据;
④指导联合治疗方案的制定,提高治疗有效率。
4.与液体活检整合的动态监测
①结合ctDNA、CTCs、尿液生物标志物,实现肿瘤进化的实时追踪;
②液体活检发现的分子异常可在匹配的PDOs中进行功能验证;
③疾病进展时可重新构建PDOs,及时调整治疗策略;
④构建"分子快照+功能验证"的动态精准医疗体系。
关于晶莱