

做肿瘤基础研究、新药研发的同行们,一定都绕不开两个扎心的行业痛点:
1. 肿瘤异质性带来的药效「体内外严重脱节」——细胞系里药效显著的候选药物,到动物模型、临床试验里频频翻车;
2. 实验重复性差——辛辛苦苦优化半年的培养体系,换个试剂批次、换个操作人员就完全重复不出来,更别说跨实验室、跨研究的结果比对。

小编最近重刷了斯坦福大学联合洛桑联邦理工学院发表在NatureMaterials上的《Next-generationcancerorganoids》文献,越读越有共鸣:这篇文章不仅戳中了当前癌症类器官技术的核心短板,更给出了下一代标准化类器官体系的完整落地路径。今天我就从实验实操、科研转化的角度,跟大家拆解清楚这篇顶刊的核心干货。
在谈「下一代」之前,我们先要明确:癌症类器官到底解决了传统模型的哪些致命缺陷?
文献里明确对比了传统肿瘤模型的核心局限(也是我们做科研踩了无数次的坑):
① 2D永生化细胞系:经过无限传代后发生克隆选择,丢失了亲本肿瘤的遗传异质性和药物应答特征,更无法模拟肿瘤三维结构与微环境,临床转化预测率极低;
② 患者来源异种移植模型(PDX):成本高、通量低、周期长,受免疫缺陷鼠的宿主选择压力,肿瘤会发生与亲本组织的遗传表型偏离,还存在严格的伦理限制。
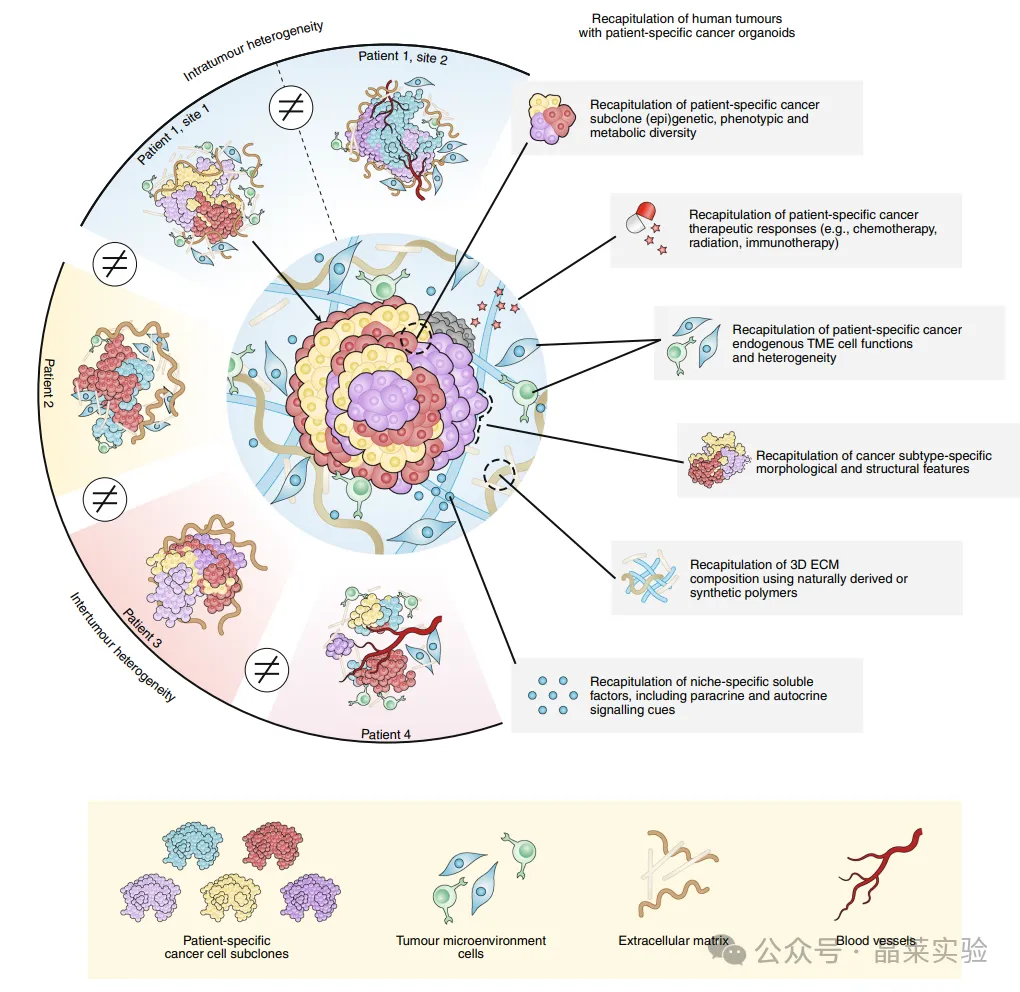
癌症器官模型再现了患者特定肿瘤异质性的关键特征
而癌症类器官,作为患者肿瘤组织来源的三维自组装细胞聚集体,恰恰精准补齐了这些短板,综述里用大量研究数据证实了它的核心价值:
1.超高的肿瘤异质性复刻能力
它能稳定保留亲本肿瘤的组织病理、遗传表观、表型特征和药物应答特性,对特定癌种的构建成功率超70%,远高于传统细胞系20%-30%的建系率。目前全球已建立了结直肠、胰腺、乳腺、卵巢、脑胶质瘤等数十种癌种的「活肿瘤生物库」,完整覆盖了不同患者的瘤间异质性,以及同一患者原发灶-转移灶的瘤内空间异质性。
2. 患者临床疗效的精准预测能力
综述中引用的胰腺癌、结直肠癌临床研究均证实:类器官的体外药物筛选结果,与患者体内临床治疗应答高度匹配。甚至可以通过类器官的药物表型特征,回溯性预测临床试验中患者的治疗获益,这是传统模型从未实现的突破。
3. 肿瘤微环境的全维度模拟能力
通过共培养体系,类器官可稳定整合癌相关成纤维细胞(CAF)、免疫细胞、内皮细胞等肿瘤微环境(TME)组分,气液界面(ALI)培养体系更是能长期保留肿瘤原生的免疫细胞库,实现免疫治疗、基质靶向药物的体外筛选,完美适配当前肿瘤靶向治疗、免疫治疗的研发需求。
既然类器官优势如此显著,为什么至今仍未完全实现临床转化的规模化落地?综述一针见血地指出:当前癌症类器官培养体系的非标准化,带来了巨大的技术差异,不仅严重影响实验重复性,更掩盖了肿瘤本身的生物学异质性。
简单来说,我们做实验时遇到的「批次差异大、结果重复不出来、机制研究说不清」,根源都在这里。文献把技术差异的来源拆解为三大核心问题,每一个都是我们实操中天天踩的坑:
1. 肿瘤组织来源与处理流程的非标准化
① 取样偏差:绝大多数类器官仅来自单次活检或手术小组织块,无法覆盖肿瘤的空间异质性,最终培养的类器官只代表了肿瘤的一小部分亚克隆;
② 处理流程混乱:是全酶解成单细胞,还是手工切碎成组织块?酶解的时间、浓度怎么定?手工切碎的片段大小不均一,直接导致氧气、营养物质传递差异,最终造成类器官生长状态、细胞组成的批次波动;
③ 污染与筛选偏差:酶解会破坏细胞表面蛋白,原生细胞间相互作用丢失,还会造成非上皮细胞、非肿瘤细胞的负向筛选;甚至有研究显示,58%的肺癌类器官会被正常气道上皮细胞过度生长,完全偏离肿瘤本身的生物学特征。
2. 培养基体系的「黑箱化」
类器官培养的核心是模拟肿瘤体内的niche微环境,但当前的培养基体系充满了不可控因素:
① 条件培养基批次差异巨大:实验室自制的Wnt、R-spondin条件培养基,不同批次的目标蛋白活性波动极大,还含有大量未知分泌因子,不可预测地影响类器官表型和药物应答;
② 动物血清的不可控性:胎牛血清(FBS)成分复杂,含有1800余种基因产物,批次间、供应商间的浓度差异极大,不仅带来异种污染风险,还会严重干扰类器官培养的稳定性;
③ 成本与稳定性矛盾:高纯度重组生长因子成本极高,且溶解性、稳定性差,多数实验室只能通过条件培养基降低成本,进一步加剧了体系的非标准化。
3.三维基质的「不可控性」,是最大的卡脖子问题
这也是NatureMaterials这篇材料顶刊最关注的核心问题。目前90%以上的类器官培养都用Matrigel(小鼠EHS肉瘤基质),但它的缺陷几乎是致命的:
① 批次间差异极大:Matrigel含有近2000种蛋白,即使是低生长因子配方,批次间蛋白相似度仅53%,不同批次的培养结果天差地别;
②力学与生化特性完全不可调:健康乳腺组织硬度约400Pa,乳腺癌组织约5kPa,而Matrigel硬度仅约100Pa,完全无法匹配肿瘤体内的基质力学特征,更无法做基质-肿瘤相互作用的机制研究;
③ 成分不明的「黑箱」:大量未知生长因子、异种蛋白,不仅干扰实验结果,还无法明确「到底是哪个基质特性调控了肿瘤表型」,机制研究根本无从谈起。
1. 样本构建全流程标准化,真正复刻肿瘤异质性
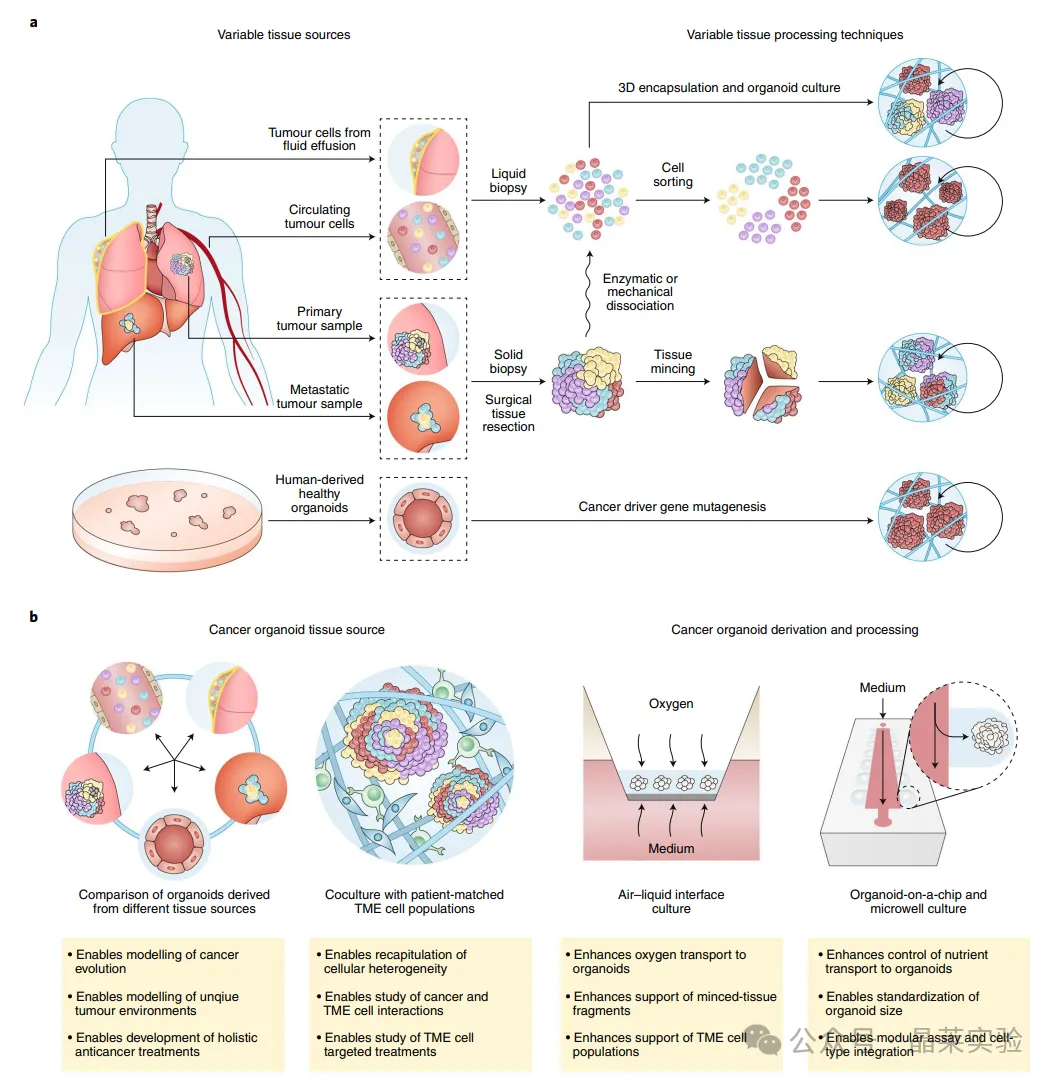
患者特定癌症器官原型的衍生过程受限于非标准化的组织获取和处理方法
① 取样与处理标准化:通过多区域取样覆盖肿瘤空间异质性,配对构建原发灶-转移灶类器官,完整保留患者肿瘤的亚克隆多样性;通过显微切割、微加工微孔阵列技术,实现组织片段尺寸、类器官初始接种细胞数的精准控制,彻底解决手工操作的批次差异;
② 突破样本时效性限制:优化冻存组织类器官构建方案,实现液氮冻存6-12个月的肿瘤组织,依然能高效构建类器官,且完整保留亲本肿瘤的药物应答特征,解决临床样本时效性的行业痛点;
③ 肿瘤微环境共培养标准化:通过气液界面(ALI)培养体系,实现肿瘤细胞与原生CAF、免疫细胞的长期稳定共培养,完整模拟肿瘤-免疫微环境的相互作用,支持免疫治疗的体外药效筛选。
2.全定义、可重复的培养基体系,彻底打破「黑箱」
① 无血清、无条件培养基的全化学定义体系:通过afamin稳定Wnt蛋白、脂质体包裹提升生长因子稳定性,实现无血清条件下的类器官稳定培养;通过原核表达体系优化,制备高活性、低内毒素的R-spondin、Gremlin1等核心蛋白,成本较市售产品降低数百倍,同时彻底消除批次差异;
② 工程化信号分子替代:采用新一代替代型Wnt/R-spondin激动剂,活性更高、成本更低,甚至可实现细胞类型特异性的通路激活,精准模拟不同肿瘤的信号通路特征;
③ 患者个性化培养基定制:不局限于肿瘤突变状态,结合单细胞转录组、蛋白组数据,为不同患者、不同癌种定制专属培养基配方,最大程度保留肿瘤原生的生物学特征。
3.工程化基质替代,实现肿瘤微环境的精准可控
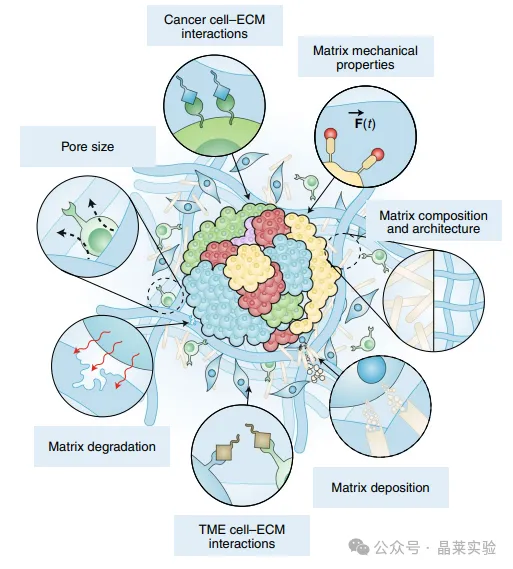
细胞外基质通过多种生化与机械相互作用调控癌症类器官表型
这是下一代类器官最核心的技术突破,也是我们实现机制研究精准化的核心工具:
① 全合成/半合成基质替代Matrigel:采用PEG合成基质、HA-ELP杂化水凝胶、纤维蛋白凝胶等工程化材料,批次间高度稳定、无动物源污染,彻底消除基质带来的技术差异;
② 基质特性的精准定制:可根据不同癌种、不同患者的肿瘤ECM特征,精准调控基质硬度、孔径、降解性、整合素配体修饰,完美匹配肿瘤体内的基质微环境,真正实现「患者特异性微环境建模」;
③ 动态基质技术:通过光控降解、光控修饰技术,实现基质生化、力学特性的时空动态调控,模拟肿瘤进展、转移过程中的基质动态重塑,解决传统静态基质无法模拟肿瘤动态演进的痛点。
这篇顶刊给整个行业指明了方向:下一代癌症类器官的核心,是通过标准化体系,消除技术带来的人为差异,真正还原肿瘤本身的生物学异质性。只有这样,类器官才能真正从实验室的「科研工具」,变成新药研发的「筛选平台」,变成临床精准医疗的「决策依据」。
我们始终坚信,标准化,才是类器官技术的生命线。从患者来源类器官(PDO)标准化构建、个性化培养基优化,到工程化基质定制化建模、高通量药物筛选,我们始终以顶刊级的标准化体系,为你的肿瘤研究保驾护航。
关于晶莱